Diagnosis dan Terapi Terkini Multiple Myeloma
Merlyna Savitri
Merlyna Savitri
Diagnosis dan Terapi Terkini Multiple Myeloma
Sumber: Medicinus Desember 2020 vol. 33 issue 3
dr. Merlyna Savitri, Sp.PD-KHOM, FINASIM
Divisi Hematologi-Onkologi Medik Departemen Ilmu Penyakit Dalam FK Unair – RSUD Dr. Soetomo Surabaya
ABSTRAK
Multiple myeloma (MM) merupakan keganasan sel plasma yang ditandai oleh proliferasi klonal sel plasma ganas di sumsum tulang dengan protein monoklonal dalam serum dan/atau urin serta disfungsi organ terkait disertai dengan morbiditas dan mortalitas substansial, berupa end-organ damage: gangguan ginjal, hiperkalsemia, lesi tulang litik, dan anemia. Dengan perkembangan terapi yang lebih baik, MM telah berubah dari penyakit yang tidak dapat diobati ke salah satu penyakit yang masih belum dapat disembuhkan, namun highly treatable dengan kebanyakan pasien dapat berobat rawat jalan. Kelangsungan hidup pada MM telah meningkat secara signifikan dalam 15 tahun terakhir. Hal ini disebabkan oleh adanya terapi terkini seperti bortezomib, thalidomide, dan lenalidomide. Dalam dekade terakhir, carfilzomib, pomalidomide, panobinostat, ixazomib, elotuzumab, daratumumab, isatuximab, dan selinexor juga telah disetujui oleh Food and Drug Administration (FDA) untuk pengobatan MM yang mengalami kekambuhan. Selain itu, adanya terapi autologous stem cell transplantation (ASCT) dapat meningkatkan median overall survival (OS) pasien MM sekitar 12 bulan dan sudah dapat dilakukan di Indonesia, khususnya di Surabaya (FK Unair-RSUD Dr. Soetomo-RS Unair).
Kata kunci: multiple myeloma, diagnosis, terapi terkini, bortezomib, ASCT
1. Pendahuluan
Multiple myeloma (MM) merupakan keganasan sel plasma yang ditandai oleh proliferasi klonal sel plasma ganas di sumsum tulang dengan protein monoklonal dalam serum dan/atau urin serta disfungsi organ terkait disertai dengan morbiditas dan mortalitas substansial, berupa end-organ damage: gangguan ginjal, hiperkalsemia, lesi tulang litik, dan anemia.1,2
Insiden MM di seluruh dunia adalah 1% dari semua kanker dan 10% dari semua keganasan hematologi. Insiden MM di Eropa adalah 4,5-6,0/100.000 per tahun, dengan median usia saat diagnosis 72 tahun; mortalitasnya adalah 4,1/100.000 per tahun. Multiple myeloma menempati peringkat ketiga setelah limfoma dan leukemia, dengan perkiraan 30.770 kasus baru (46,7% perempuan; 53,3% laki-laki) didiagnosis setiap tahunnya di Amerika Serikat.3
Hampir semua pasien dengan MM berevolusi dari stadium asimtomatik praganas yang disebut gamopati monoklonal dengan signifikansi yang tidak dapat ditentukan (monoclonal gammopathy of undetermined significance/MGUS). MGUS berkembang menjadi MM dengan laju 1% per tahun. Pada sebagian pasien, dapat dijumpai kondisi asimtomatik intermediate yang lebih mengarah pada tahap praganas yang disebut smoldering (atau indolent) MM (SMM). Smoldering MM berkembang menjadi MM dengan laju 10% per tahun selama 5 tahun pertama setelah diagnosis, 3% per tahun selama 5 tahun berikutnya, dan 1,5% per tahun sesudahnya.4
Multiple myeloma merupakan penyakit yang unik karena tes diagnostik dasarnya hanya mencakup sel darah lengkap dengan hitung diferensial, panel metabolik dasar; serum kalsium, serum dan elektroforesis protein urin; serta bone survey yang semuanya seharusnya dapat diakses di negara-negara berpenghasilan rendah dan menengah. Beberapa tes lanjutan, seperti free light-chain assay (FLC), pemindaian tomografi (fluorodeoxyglucose-positron emission tomography/ FDG-PET), pemeriksaan sitogenetik, dan fluorescence in situ hybridization (FISH) mungkin masih lebih terbatas dan tidak tersedia di semua negara.
Dengan perkembangan terapi yang lebih baik, MM telah berubah dari penyakit yang tidak dapat diobati ke salah satu penyakit yang masih belum dapat disembuhkan tetapi dapat diobati(highly treatable) dengan terapi kebanyakan pasien rawatjalan.Perkembangan pengobatan MM telah meningkat secara substansial selama dekade terakhir. Kemajuan besar pertama adalah pengembangan transplantasi sel punca autologous (autologous stem cell transplant/ASCT) pada tahun 1980-an dan 1990-an. Beberapa agen terapi yang tergolong baru dikembangkan pada akhir tahun 1990-an dan di awal tahun 2000-an, dimulai dengan “IMIDs” (thalidomide dan lenalidomide) kemudian diikuti oleh proteasome inhibitors (PIs). Baru-baru ini, antibodi monoklonal, seperti daratumumab dan elotuzumab, serta agen histone deacetylating, seperti panobinostat, juga telah mendapatkan persetujuan dari Food and Drug Administration (FDA) untuk tata laksana MM.2
Selama beberapa dekade, terapi standar untuk MM adalah kombinasi agen alkilasi, terutama melphalan dan cyclophosphamide, bersama dengan corticosteroid, seperti dexamethasone dan prednisone, diikuti pada pertengahan 1980-an dengan diperkenalkannya transplantasi sel induk autologous. Dalam 20 tahun terakhir, sejak adanya penemuan manfaat immunomodulatory dari thalidomide di akhir 1990-an, tampak pergeseran yang bermakna dalam ketersediaan pilihan terapi untuk mengobati MM. Perkembangan berikutnya diikuti oleh pengenalan imunomodulator tambahan (IMiDs) lenalidomide dan pomalidomide, lalu golongan proteasome inhibitor seperti bortezomib, , dan ixazomib, serta histone deacetylase (HDAC) inhibitor panobinostat. Selanjutnya pada akhir tahun 2015, dua buah antibodi monoklonal, daratumumab dan elotuzumab, yang merupakan targeted therapy terhadap CD38 dan antigen SLAMF7 yang ditemukan pada permukaan sel myeloma, mendapatkan persetujuan izin edar. Perkembangan ini telah menghasilkan peningkatan tingkat kelangsungan hidup 5 tahun (5-year survival) penderita MM hampir dua kali lipat menjadi 50% dalam 30 tahun.3
Pengobatan standar untuk MM sangat bergantung pada kebugaran pasien dan baseline status kesehatannya. Bagi mereka yang berada dalam kondisi sehat dan berusia lebih muda dari 70 hingga 75 tahun, pengobatan yang lebih disukai untuk pasien yang baru terdiagnosis dengan myeloma terdiri regimen triplet agen barus , biasanya mencakup IMID dan PI dalam kombinasi dengan diikuti autologous stem cell transplantation (ASCT) dan terapi pemeliharaan dengan IMID dosis rendah atau PI. Bagi mereka yang tidak dapat menjalani ASCT, terapi standar mencakup induksi dengan agen baru dilanjutkan dengan terapi pemeliharaan dosis rendah.2
Tata laksana dengan autologous peripheral blood stem cell transplant (PBSCT) bukanlah hal yang baru di dunia karena telah dipraktikkan sejak tahun 1980-an, namun di Indonesia tindakan ini dapat terbilang sangat baru. Negara dengan tingkat ketersediaan transplantasi sel induk tertinggi (untuk semua indikasi termasuk MM) adalah Israel (814), Italia (671), Jerman (665), Swedia (625), dan Belanda (614) per 10 juta penduduk.2
Pada kasus MM, ASCT meningkatkan progression-free survival (PFS) dan overall survival (OS) dibandingkan dengan modalitas kemoterapi saja. Saat ini, Amerika Serikat melakukan sekitar 10.000 ASCT per tahun dengan metode peripheral blood stem cell transplant (PBSCT).5 Di Indonesia, ASCT juga sudah dapat dilakukan di beberapa center. Di Surabaya (FK Unair-RSUD Dr. Soetomo-RS Unair) telah dilakukan 14 kali ASCT dengan metode PBSCT sejak tahun 2014.
1. Definisi
dilakukan 14 kali ASCT dengan metode PBSCT sejak tahun 2014. Multiple Myeloma (MM) adalah keganasan sel plasma yang diperoleh dari sebuah klon tunggal. Keganasan ini ditandai adanya kerusakan skeletal, gagal ginjal, anemia, dan hiperkalsemia.6 Pematangan dan proliferasi limfosit B matang menjadi sel plasma pada keadaan normal distimulasi oleh paparan tubuh terhadap antigen dan selanjutnya sel plasma tersebut akan melepaskan imunoglobulin yang ikut berperan dalam respons imun adaptif humoral, namun pada kasus MM kontrol terhadap proses ini hilang. Sel ganas akan terakumulasi pada sumsum tulang dan memproduksi imunoglobulin yang abnormal. Keberadaan tumor itu sendiri, produk yang dikeluarkan oleh sel tumor (imunoglobulin), dan respons tubuh terhadap sel tumor menyebabkan berbagai gejala disfungsi organ seperti nyeri tulang, patah tulang, gagal ginjal, kerentanan terhadap infeksi, anemia, hiperkalsemia, gangguan koagulasi, gejala neurologis, dan hiperviskositas darah beserta manifestasinya.7
2. Insiden
American Cancer Society memperkirakan kasus MM baru yang terdiagnosis di Amerika Serikat (AS) pada tahun 2017 mencapai 30.280 kasus, dengan jumlah kematian karena MM sebesar 12.590 selama kurun waktu tersebut. Data di AS menunjukkan bahwa myeloma memiliki insiden sebesar 1,3% dari semua keganasan pada orang kulit putih, dan sebesar 2% dari semua keganasan pada orang kulit hitam. Data tersebut juga menyebutkan bahwa MM memiliki insiden sebesar 13% dari semua keganasan hematologi pada orang kulit putih dan 33% dari semua keganasan hematologi pada orang kulit hitam.8
Insiden MM berbanding lurus dengan usia, dengan median usia pada saat diagnosis adalah 70 tahun. MM jarang terjadi pada orang yang berusia di bawah 40 tahun dan insidennya lebih sering pada pria dibandingkan dengan wanita. Insiden MM pada orang kulit hitam jumlahnya dua kali lipat dibandingkan pada orang kulit putih. Insiden MM tertinggi dijumpai pada ras Amerika Afrika serta penduduk di kepulauan Pasifik dan tidak terlalu banyak pada orang kulit putih Eropa dan Amerika Utara. Insiden MM sangat rendah di negara berkembang termasuk negara-negara Asia seperti di Cina dan Jepang. Karakteristik penyakit, respons terhadap terapi, dan prognosis MM dilaporkan sama di seluruh dunia, meskipun insiden antarpopulasi di berbagai negara di belahan dunia menunjukkan beberapa perbedaan.9
3. Etiologi
Penyebab MM tidak diketahui secara pasti. Hubungan antara risiko terjadinya myeloma dengan faktor lingkungan, seperti radiasi, paparan racun kimia oleh industri atau pertanian masih belum jelas. Abnormalitas sitogenetik dan onkogen terjadi pada sebagian besar penderita myeloma, yaitu DNA hiperploidi pada 75% penderita dan abnormalitas multipel pada setiap kariotipe. Delesi komplit atau delesi parsial pada kromosom 13 merupakan penanda prognosis yang buruk. Variasi kelainan kromosom pada pasien MM antara lain: hiperdiploid, delesi 13q14, translokasi t(11;14)(q13;q32), t(4;14)(p16;q32), dan t(14;16), serta delesi 17p13. Bukti-bukti yang ada menunjukkan bahwa kesalahan rekombinasi saat mengganti isotipe rantai berat antibodi, berperan pada proses transformasi tersebut.10
Frekuensi kejadian MM meningkat pada orang yang terpapar senjata nuklir pada saat perang dunia II setelah melalui periode laten selama 20 tahun. MM lebih sering terjadi pada petani, tukang kayu, pengrajin kulit, dan orang yang terpapar produk petroleum. Sampai saat ini belum ada jalur biomolekular yang bisa menjelaskan hal tersebut. Penelitian tentang urutan genom belum berhasil mengidentifikasi adanya mutasi recurrent dengan frekuensi lebih dari 20%. Mutasi NRAS, KRAS, dan BRAF merupakan mutasi yang paling sering terjadi. Kombinasi mutasi tersebut jika dikombinasikan mencakup 40% pasien dari semua pasien MM.7
5. Gambaran Klinis
5.1 Anamnesis
Multiple Myeloma (MM) secara klinis memiliki gejala yang terangkum dalam istilah CRAB. CRAB merupakan akronim dari gejala-gejala MM berupa hypercalcemia, renal failure, anemia, dan lytic bone lession.11 Nyeri tulang adalah gejala yang paling sering dikeluhkan oleh pasien MM, dan gejala ini dijumpai pada 70% dari seluruh pasien MM. Nyeri pada kasus MM dipresipitasi oleh gerakan. Hal ini berbeda dengan nyeri pada metastasis karsinoma yang karakteristik nyerinya tidak dipresipitasi oleh gerakan dan terutama terjadi pada malam hari. Nyeri yang terlokalisasi dan terjadi secara persisten dapat merupakan pertanda adanya fraktur patologis.7
Manifestasi klinis lain yang sering terjadi pada pasien MM adalah kerentanan terhadap infeksi bakteri. Infeksi yang paling sering terjadi adalah pneumonia dan pielonefritis. Patogen yang paling sering menginfeksi pasien MM di paru adalah Streptococcus pneumoniae, Staphylococcus aureus, dan Klebsiella pneumoniae, sementara patogen di saluran kemih adalah Escherichia coli dan organisme Gram negatif lainnya. Infeksi berulang terjadi pada 25% pasien MM dan >75% pasien MM pernah mengalami infeksi serius sebanyak satu kali selama menderita MM. Terdapat beberapa faktor penyebab yang berkontribusi pada kerentanan pasien MM pada infeksi. Pasien dengan MM memiliki hipogamaglobulinemia difus (dihitung tanpa mengikutsertakan komponen M). Hipogamaglobulinemia yang terjadi disebabkan oleh menurunnya produksi dan meningkatnya destruksi antibodi normal. Selain itu pada beberapa pasien juga muncul sel regulator yang mensupresi sintesis antibodi normal. Komponen M yang berlebihan menyebabkan terjadinya katabolisme antibodi yang meningkat. Pasien MM sebenarnya memiliki fungsi sel T yang normal, namun jumlah subset CD4 menurun. Lisozim yang terdapat pada granulosit jumlahnya menurun dan migrasi granulosit melambat, tidak secepat pada orang normal. Seluruh faktor tersebut berkontribusi terhadap timbulnya defisiensi imun pada pasien MM. Di samping hal tersebut, beberapa pasien juga menggunakan agen terapeutik seperti dexamethasone yang memiliki efek supresi respons imun sehingga turut meningkatkan kerentanan terhadap infeksi bakteri dan jamur.7
Gejala neurologis relatif hanya terjadi pada sedikit pasien MM. Gejala neurologis ini memiliki berbagai macam sebab. Hiperkalsemia dapat menyebabkan letargi, kelemahan tubuh, depresi, dan confusion. Hiperviskositas dapat menyebabkan sakit kepala, fatigue, sesak napas, eksaserbasi gagal jantung, gangguan visual, ataksia, vertigo, retinopati, somnolence, dan koma. Kerusakan dan kolaps tulang belakang dapat menyebabkan kompresi spinal, nyeri radikular, serta hilangnya kontrol berkemih dan defekasi. Infiltrasi saraf perifer oleh amiloid dapat menyebabkan carpal tunnel syndrome, mononeuropati, maupun polineuropati sensorimotor lainnya.7
5.2 Pemeriksaan Fisik
Pemeriksaan fisik pada pasien yang diduga menderita MM dilakukan untuk mencari nyeri tulang dan massa, serta tanda-tanda anemia.
5.3 Pemeriksaan Laboratorium
Peningkatan kreatinin serum terjadi pada hampir 50% pasien MM. Lebih dari 20% pasien MM memiliki kreatinin serum >2 mg/dl. Banyak faktor yang berkontribusi pada kejadian gagal ginjal tersebut. Penyebab tersering gagal ginjal pada pasien MM adalah myeloma kidney (presipitasi rantai ringan monoklonal pada tubulus distal dan tubulus kolektikus) dan hiperkalsemia. Penyebab gagal ginjal lain pada pasien MM antara lain deposit amiloid pada glomerulus, hiperurisemia, infeksi berulang, penggunaan nonsteroid anti-inflamatory drugs (NSAIDs) yang terlalu sering untuk mengatasi nyeri, penggunaan kontras untuk pemindai, penggunaan bisphosphonate, dan terkadang terjadi infiltrasi sel myeloma pada ginjal. Kerusakan tubular akibat ekskresi light chain hampir selalu terjadi.12
Anemia normokromik normositik terjadi pada 73% pasien MM. Anemia dapat terjadi melalui beberapa mekanisme, antara lain defisiensi eritropoietin akibat adanya gagal ginjal dan pendesakan sel tumor pada sumsum tulang normal. Anemia hemolisis ringan juga berkontribusi terhadap terjadinya anemia namun tergolong jarang.12 Sel tumor juga menyebabkan produksi sitokin yang mensupresi sumsum tulang.13,14 Anemia juga dapat terjadi sebagai akibat dari terapi jangka panjang yang diberikan. Anemia megaloblastik dapat terjadi karena defisiensi asam folat dan vitamin B12. Granulositopenia dan trombositopenia dapat terjadi namun tergolong jarang dan biasanya diinduksi oleh terapi yang diberikan. Abnormalitas pembekuan darah dapat terjadi karena adanya antibodi yang melingkupi platelet sehingga platelet tidak bisa berfungsi sebagaimana mestinya. Abnormalitas pembekuan darah dapat terjadi karena adanya interaksi komponen M dengan faktor koagulasi I, II, V, VII, atau VIII. Antibodi terhadap faktor koagulasi dan kerusakan endotelium akibat amiloid juga berperan dalam kejadian pembekuan darah yang abnormal.7
Pemeriksaan radiografi dada dan tulang dapat menunjukkan adanya lesi litik atau osteopenia difus. Pemeriksaan darah lengkap dapat menunjukkan adanya anemia dan peningkatan laju endap darah (LED). Kadar kalsium serum, urea nitrogen serum, kreatinin serum, dan asam urat serum dapat meningkat. Elektroforesis protein (ELP) serum atau urin berguna untuk mendeteksi dan mengidentifikasi adanya M spikes. Pengukuran imunoglobulin dan rantai ringan bebas spesimen urin 24 jam diperlukan untuk menghitung jumlah ekskresi protein Bence Jones. Pengukuran mikroglobulin β2 dan albumin juga perlu dilakukan untuk menilai prognosis.7
6. Diagnosis
Kriteria diagnosis MM dari International Myeloma Working Group (IMWG) yang telah direvisi, beserta kelainan-kelainan yang berhubungan dengan MM ditunjukkan pada tabel 1. Diagnosis MM ditegakkan dengan adanya plasmasitosis (≥10%) pada pemeriksaan sumsum tulang atau pada plasmasitoma melalui biopsi ditambah bukti adanya satu atau lebih MDE (myeloma defining event), yaitu CRAB (hypercalcemia, renal failure, anemia, dan lytic bone lession) yang sudah ditegakkan serta tiga biomarker spesifik: sel plasma sumsum tulang klonal ≥60%, rasio serum free light chain (FLC) ≥100 (FLC ≥100 mg/l), dan terdapat 1 atau lebih lesi fokal pada MRI (dengan ukuran minimal 5 mm). Dalam beberapa studi, setiap biomarker baru tersebut berasosiasi dengan sekitar 80% risiko perkembangan penyakit ke arah kerusakan organ target. Kriteria yang telah direvisi ini menunjukkan pergeseran paradigma yang memungkinkan diagnosis lebih dini serta dimulainya terapi sebelum terjadi end-organ damage. 11,15
Ketika MM dicurigai secara klinis, pasien harus menjalani tes untuk memeriksa keberadaan protein M menggunakan kombinasi tes yang harus mencakup elektroforesis protein serum (serum protein electrophoresis/SPEP), imunofiksasi serum (serum immunofixation/SIFE), dan uji FLC serum. Sekitar 2% dari pasien MM memiliki penyakit nonsekretorik yang sesungguhnya dan tidak memiliki bukti protein M. Studi sumsum tulang pada saat diagnosis awal harus mencakup probe fluorescent in situ hybridization (FISH) yang dirancang untuk mendeteksi t(11;14), t(4;14), t(14;16), t(6;14), t(14;20), trisomi, dan del (17p). Karyotyping konvensional untuk mendeteksi hipodiploidi dan delesi 13 memiliki nilai, tetapi jika FISH telah dilakukan, nilai tambahan dalam stratifikasi risiko awal terbatas. Jika tersedia, gene expression profiling (GEP) dapat memberikan nilai prognostik tambahan. Serum CrossLaps untuk mengukur carboxy-terminal collagen crosslinks (CTX) mungkin berguna dalam menilai turnover tulang dan untuk menentukan kecukupan terapi bisphosphonate. Cara terbaik untuk menilai gangguan pada tulang adalah dengan pencitraan WB-CT atau PET/CT dosis rendah. MRI berguna pada pasien dengan dugaan SMM untuk memeriksa lesi sumsum tulang fokal yang dapat dilihat sebelum penyakit osteolitik yang sesungguhnya terjadi. Selain itu, pencitraan MRI berguna dalam menilai adanya penyakit ekstrameduler, dugaan kompresi sumsum tulang, atau ketika pencitraan rinci dari area simtomatik diperlukan. Survei skeletal konvensional kurang sensitif dibandingkan WB-CT dan PET/CT dosis rendah dan hanya direkomendasikan jika metode pencitraan yang lebih lanjut tidak tersedia. Protein M dikategorikan terukur jika bernilai ≥1 g/dl dalam serum dan/atau ≥200 mg/hari dalam urin. Kadar protein M dipantau dengan SPEP dan uji FLC serum untuk menilai respons pengobatan setiap bulan selama terapi, dan setiap 3-4 bulan saat tidak dalam masa terapi. Uji FLC serum sangat berguna pada pasien yang kekurangan protein M yang dapat diukur, di mana rasio FLC abnormal dan tingkat FLC yang terlibat adalah ≥100 mg/l. Elektroforesis protein urin direkomendasikan untuk dilakukan setidaknya sekali setiap 3-6 bulan, untuk memantau kadar protein M urin serta untuk mendeteksi komplikasi ginjal lain yang dapat menyebabkan albuminuria. 11,15
Tabel 1. Kriteria diagnostik MM dari IMWG11,15

7. Klasfisikasi Molekuler
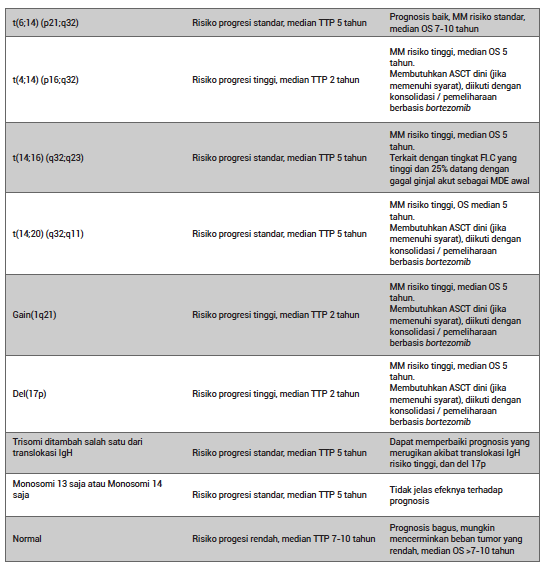
Meskipun multiple myeloma (MM) masih dianggap sebagai penyakit tunggal, pada kenyataannya penyakit ini merupakan kumpulan dari beberapa keganasan sel plasma yang berbeda secara sitogenetik. Pada studi FISH tentang sumsum tulang, sekitar 40% dari MM ditandai oleh adanya trisomi dalam sel plasma neoplastik (multiple myeloma trisomik), sedangkan sebagian besar sisanya memiliki translokasi yang melibatkan lokus rantai berat imunoglobulin (IgH) pada kromosom 14q32 (IgH mentranslokasi MM). Sebagian kecil pasien mengalami trisomi dan translokasi IgH. Translokasi trisomi dan IgH dianggap sebagai kelainan sitogenetik primer dan terjadi pada saat pembentukan MGUS. Selain itu, perubahan sitogenetik lain yang disebut kelainan sitogenetik sekunder muncul di sepanjang perjalanan penyakit MM, termasuk gain(1q), del(1p), del(17p), del(13), mutasi RAS, dan translokasi sekunder yang melibatkan MYC. Baik kelainan sitogenetik primer dan sekunder dapat memengaruhi perjalanan penyakit, respons terhadap terapi, serta prognosis. Interpretasi dan dampak kelainan sitogenetik yang bermakna pada MM bervariasi tergantung pada fase penyakit di mana kelainan tersebut terdeteksi (tabel 2).15
Tabel 2. Pengaruh Abnormalitas Sitogenetik terhadap Perjalanan Penyakit dan Prognosis MM15

8. Stadium
Pasien dengan MM aktif dikategorikan menurut sistem staging Durie-Salmon (tabel 3) atau International Staging System (ISS) (tabel 4). Sistem staging Durie-Salmon didasarkan pada densitas sel tumor pada sumsum tulang, pengukuran kerusakan end-organ ginjal, anemia, hiperkalsemia, lesi tulang litik), serta kadar immunoglobulin. 16,17
Tabel 3. Sistem staging Durie-Salmon17

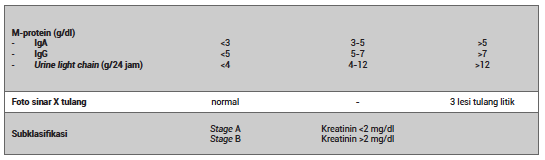
Sistem ISS didasarkan pada kadar mikroglobulin β2 dan albumin serum, terbagi menjadi 3 kelompok yang memiliki signifikansi prognostik yang berbeda-beda. Dibanding dengan sistem staging Durie-Salmon, ISS memiliki parameter laboratorium yang lebih mudah diperoleh. Sistem ISS juga dapat memprediksi prognostik dan OS.16
Tabel 4. International Staging System (ISS)16

IMWG baru-baru ini mengembangkan sistem ISS yang direvisi (Revised International Staging System/R-ISS) yang dianggap lebih mampu memprediksi prognosis dibanding sistem ISS sebelumnya. R-ISS memasukkan faktor-faktor yang sebelumnya sudah ada dalam ISS (kadar mikroglobulin β2 dan albumin serum) ditambah dengan kadar LDH serum serta abnormalitas kromosom risiko tinggi seperti yang terlihat pada tabel 5.18
Tabel 5. Revised International Staging System (R-ISS)18

Perkiraan kelangsungan hidup pada multiple myeloma bervariasi berdasarkan sumber datanya. Data dari uji coba acak terkontrol menggunakan terapi modern menunjukkan bahwa rata-rata kelangsungan hidup pada multiple myeloma adalah sekitar 6 tahun. Pada pasien yang memenuhi syarat untuk ASCT, tingkat kelangsungan hidup 4 tahun lebih dari 80%; rata-rata kelangsungan hidup keseluruhan (overall survival/OS) di antara pasien ini adalah sekitar 8 tahun. Pada pasien berusia lanjut (>75 tahun), median OS lebih rendah, yakni sekitar 5 tahun.15
Estimasi prognosis yang lebih tepat memerlukan penilaian berbagai faktor. Seperti pada kanker lain, OS pada multiple myeloma dipengaruhi oleh karakteristik host, beban tumor (stadium), biologi (kelainan sitogenetik), dan respons terhadap terapi. Beban tumor pada multiple myeloma secara tradisional dinilai menggunakan Durie-Salmon Staging (DSS) dan International Staging System (ISS). Biologi penyakit paling baik direfleksikan berdasarkan subtipe molekuler multiple myeloma, ada atau tidak adanya kelainan sitogenetik sekunder seperti del(17p), gain(1q), atau del(1p) seperti dijelaskan pada tabel 2. Selain faktor risiko sitogenetik, dua penanda lain yang terkait dengan biologi penyakit agresif adalah peningkatan serum lactate dehydrogenase (LDH), dan bukti sel plasma yang bersirkulasi pada pemeriksaan apusan perifer rutin (leukemia sel plasma). The Revised International Staging System (R-ISS) menggabungkan elemen beban tumor (ISS) dan biologi penyakit (adanya kelainan sitogenetik berisiko tinggi atau peningkatan lactate dehydrogenase), untuk membuat indeks prognostik terpadu yang membantu dalam perawatan klinis serta sebagai perbandingan data uji klinik seperti dijelaskan pada tabel 5. Jika MM ditangani dengan tepat, kelangsungan hidup pasien dengan kategori risiko tinggi tertentu dapat mendekati pasien MM dengan penyakit risiko standar.15
9. Terapi
Sekitar 10% pasien MM memiliki progresivitas penyakit yang sangat lambat (disebut smoldering myeloma) dan tidak memerlukan terapi. Terapi baru dimulai ketika kadar paraprotein meningkat di atas 5 g/dl atau terjadi penyakit tulang progresif. Pasien dengan MM simtomatik atau progresif memerlukan intervensi terapeutik. Terapi yang diberikan dapat memperpanjang survival pasien MM secara signifikan.7
Kelangsungan hidup pada MM telah meningkat secara signifikan dalam 15 tahun terakhir. Dampak awal berasal dari diperkenalkannya thalidomide, bortezomib, dan lenalidomide. Dalam dekade terakhir, , pomalidomide, panobinostat, ixazomib, elotuzumab, daratumumab, isatuximab, dan selinexor telah disetujui oleh Food and Drug Administration (FDA) untuk pengobatan MM yang kambuh, dan dapat untuk meningkatkan hasil lebih lanjut. Banyak kombinasi telah dikembangkan dengan menggunakan obat yang menunjukkan aktivitas pada MM, dan regimen yang paling umum digunakan tercantum dalam tabel 6. Obat-obat yang digunakan dalam tata laksana MM bekerja melalui berbagai mekanisme, beberapa di antaranya tidak sepenuhnya dipahami. Thalidomide, lenalidomide, dan pomalidomide disebut agen imunomodulator (IMiDs); mereka berikatan dengan cereblon dan mengaktifkan aktivitas cereblon E3 ligase. Hal ini menghasilkan ubiquitination yang cepat dan degradasi dari dua faktor transkripsi sel B spesifik, Ikaros family zinc finger proteins Ikaros (IKZF 1) dan Aiolos (IKZF3). Obat ini dapat menyebabkan sitotoksisitas langsung dengan menginduksi kerusakan DNA yang dimediasi oleh radikal bebas. Selain itu, obat ini juga memiliki sifat antiangiogenesis, penghambatan tumor necrosis factor alpha (TNF-α), dan efek imunomodulator. , dan ixazomib adalah golongan proteasome inhibitor. Elotuzumab adalah terapi tertarget yang bekerja pada SLAMF7; daratumumab dan isatuximab bekerja pada target CD38; sementara panobinostat adalah suatu deacetylase inhibitor.15
Secara umum, terapi yang digunakan untuk tata laksana MM terbagi menjadi dua golongan berdasarkan tujuan pemberiannya, yaitu terapi sistemik untuk mengendalikan progresivitas MM dan terapi suportif simtomatik untuk mencegah morbiditas dari komplikasi yang ditimbulkan oleh MM.7,15
9.1 Terapi sistemik untuk mengendalikan progresivitas MM
Terapi yang diberikan dapat dilakukan melalui beberapa pendekatan. Salah satu pendekatan yang umum adalah berdasarkan pada apakah seorang pasien merupakan kandidat transplantasi sel punca autologous (autologous stem cell transplantation/ASCT) atau bukan. Pasien yang merupakan kandidat transplantasi sebaiknya menghindari alkylating agent.
9.1.1 Terapi awal pada pasien MM yang memenuhi syarat untuk ASCT
Umumnya pasien dirawat dengan sekitar 3-4 siklus terapi induksi sebelum pengambilan sel punca. Setelah panen, pasien dapat menjalani ASCT frontline atau melanjutkan terapi induksi, menunda ASCT hingga kambuh pertama. Ada banyak pilihan untuk terapi awal yang juga dapat digunakan pada saat kambuh. Secara umum, regimen dexamethasone dosis rendah (40 mg sekali seminggu) lebih disukai di semua regimen untuk meminimalisasi toksisitas. Dalam uji coba acak yang dilakukan oleh Eastern Cooperative Oncology Group (ECOG), pendekatan pendekatan dexamethasone dosis rendah dikaitkan dengan OS yang superior dan toksisitas yang secara signifikan lebih rendah.15
Bortezomib, lenalidomide, dexamethasone (VRd) adalah standar perawatan terkini untuk multiple myeloma yang baru didiagnosis. Dalam uji coba acak yang dilakukan oleh Southwest Oncology Group (SWOG), tingkat respon, PFS, dan OS secara signifikan lebih unggul dengan regimen VRd dibandingkan dengan lenalidomide dan dexamethasone (Rd). Pengumpulan sel punca dengan faktor perangsang granulosit (granulocyte-colony stimulating factor/G-CSF) saja mungkin terganggu ketika lenalidomide digunakan sebagai terapi induksi. Pasien yang telah menerima lebih dari 4-6 siklus lenalidomide mungkin membutuhkan plerixafor untuk mobilisasi sel punca. Semua pasien yang diobati dengan lenalidomide memerlukan profilaksis dengan antitrombotik. Aspirin cukup adekuat untuk sebagian besar pasien, namun pada pasien yang berisiko tinggi mengalami trombosis, diperlukan heparin atau warfarin dengan berat molekul rendah. Jika lenalidomide tidak tersedia untuk digunakan sebagai obat awal terapi atau dengan adanya gagal ginjal akut, regimen lain yang mengandung bortezomib seperti bortezomib-thalidomide-dexamethasone (VTd) atau bortezomib-cyclophosphamide-dexamethasone (VCd) dapat digunakan sebagai alternatif VRd. Penelitian baru-baru ini menemukan bahwa VTd menghasilkan tingkat respons yang lebih tinggi dibandingkan dengan VCd, namun dampaknya pada hasil jangka panjang tidak diketahui. Daratumumab, lenalidomide, dexamethasone (DRd) telah menunjukan aktivitas yang signifikan pada pasiem MM yang bukan kandidat tranplantasi, dan merupakan alternatif tambahan untuk VRd. Dalam studi awal, neuropati perifer merupakan perhatian utama pada terapi bortezomib. Neuropati pada pemberian bortezomib dapat terjadi secara tiba-tiba, dan dapat sangat menyakitkan atau melemahkan. Akan tetapi neurotoksisitas bortezomib dapat sangat dikurangi dengan pemberian bortezomib sekali seminggu daripada dua kali seminggu, dan dengan pemberian obat dengan rute subkutan dibandingkan intravena. Jadwal bortezomib subkutan sekali seminggu telah membuat neuropati serius menjadi masalah yang tidak umum, dan telah membuat regimen VRd, VCd, dan VTd jauh lebih dapat ditoleransi. Bortezomib tampaknya tidak memiliki efek merugikan pada mobilisasi sel punca. Dua buah studi fase II melaporkan hasil dengan bila digunakan dalam kombinasi dengan lenalidomide dan dexamethasone untuk MM yang baru didiagnosis. Namun terdapat kekhawatiran risiko yang lebih besar untuk terjadinya toksisitas serius dengan , sehingga lebih banyak data dibutuhkan. Penelitian di Amerika Serikat (ENDURANCE) saat ini sedang berlangsung yang bertujuan untuk membandingkan regimen VRd dan KRd sebagai terapi awal.15
Hasil pengujian regimen quadruplet yang mengandung daratumumab, suatu antibodi monoklonal yang menargetkan CD38 cukup menjanjikan. Dalam satu percobaan acak, daratumumab, bortezomib, thalidomide, dexamethasone (Dara-VTd) menunjukkan tingkat respons yang superior, kelangsungan hidup bebas progresi penyakit (progression-free survival/PFS), dan kecenderungan OS yang lebih baik dibandingkan dengan VTd. Penelitian fase II yang diacak menemukan bahwa penambahan daratumumab pada regimen VRd meningkatkan kecepatan dan kedalaman respons terhadap terapi. Dalam penelitian ini, seperti yang diharapkan, manfaat daratumumab dalam endpoint pengganti lebih menonjol pada pasien risiko standar, namun efek positif terlihat baik dalam kelompok berisiko standar maupun tinggi. Data fase III tentang manfaat PFS dan OS tambahan menggunakan regimen quadruplet melebihi standar VRd saat ini sedang ditunggu. Oleh karena itu, sangat bijaksana untuk membatasi penggunaan regimen quadruplet untuk pasien yang memenuhi syarat transplantasi dengan MM double atau triple hit berisiko tinggi, hingga terdapat data OS yang jelas untuk memastikan penambahan potensi biaya dan risiko jangka panjang pada pasien berisiko standar yang menunjukkan hasil yang sangat baik dengan triplet VRd.15
Selain regimen yang dibahas di atas, pilihan lain termasuk regimen yang mengandung anthracycline seperti bortezomib, doxorubicin, dexamethasone (PAD) atau regimen kemoterapi kombinasi multiagen, seperti VDT-PACE (bortezomib, dexamethasone, thalidomide, cisplatin, doxorubicin, cyclophosphamide, etoposide). Regimen ini sangat berguna pada pasien dengan penyakit agresif seperti leukemia sel plasma atau multiple extramedullary plasmacytomas. 15
Salah satu regimen kemoterapi bagi pasien MM kandidat transplantasi yang tersedia di Indonesia dan dapat ditanggung oleh BPJS adalah VAD. Regimen VAD terdiri dari kombinasi 4 hari infus kontinu vincristine (0,4 mg/hari) dan doxorubicin (7 mg/m2 ) yang diberikan melalui kateter vena sentral disertai pemberian dexamethasone intermitten (40 mg setiap pagi selama 4 hari). Regimen VAD diberikan dengan interval 4 minggu. Tingkat respons pasien dengan regimen VAD berkisar di angka 55%. Durasi respons pasien refractory MM yang menggunakan regimen VAD memiliki median survival sekitar 9 bulan.20
9.1.2 Terapi pada pasien MM yang tidak memenuhi syarat untuk ASCT
Pada pasien dengan multiple myeloma yang baru didiagnosis dan bukan kandidat untuk ASCT karena faktor usia atau penyakit penyerta lainnya, pilihan utama untuk terapi awal adalah VRd dan DRd. Meskipun regimen berbasis melphalan telah diuji secara ekstensif pada kelompok pasien ini, melphalan tidak direkomendasikan karena adanya kekhawatiran tentang kerusakan sel punca dan risiko sindrom myelodysplastic sekunder serta leukemia. Di Amerika Serikat, kelayakan transplantasi tidak ditentukan oleh batasan usia yang ketat, dan banyak pasien yang terdaftar dalam uji klinik berbasis melphalan akan digolongkan sebagai kandidat ASCT. 15
Terapi dengan VRd telah menunjukkan manfaat perpanjangan survival dibandingkan dengan Rd, dan merupakan pilihan yang lebih disukai untuk terapi awal pada pasien yang bukan kandidat ASCT. VRd diberikan selama sekitar 8-12 siklus, diikuti dengan terapi pemeliharaan. Jika terapi awal dengan VRd tidak memungkinkan, terutama karena alasan logistik (seperti masalah kepatuhan karena kebutuhan untuk pemberian parenteral), ixazomib dapat dipertimbangkan sebagai alternatif bortezomib. Pada pasien lanjut usia yang lemah, dosis lenalidomide yang lebih rendah harus digunakan; dexamethasone dapat dimulai dengan 20 mg sekali seminggu, kemudian dikurangi sebanyak mungkin setelah 4-6 siklus pertama, dan dihentikan setelah tahun pertama.15
Regimen berbasis melphalan hanya dipertimbangkan jika terdapat kendala akses untuk lenalidomide. Risiko melphalan dapat dikurangi dengan menggunakan cyclophosphamide sebagai gantinya, dan penelitian menunjukkan substitusi ini tidak mengubah efikasi. Oleh karena itu, regimen VCd dapat dianggap sebagai modifikasi kecil dari regimen VMP, di mana cyclophosphamide digunakan sebagai alkylating agent menggantikan melphalan. Variasi ini memiliki keuntungan karena tidak memengaruhi mobilisasi sel induk, dan pemberian dosis lebih dapat diprediksi. Sebuah uji coba acak fase III menemukan PFS dan OS yang lebih unggul dengan regimen empat obat DaraVMP dibandingkan dengan VMP, tetapi kontribusi daratumumab terhadap komponen induksi tidak dapat dipastikan dari studi ini.15
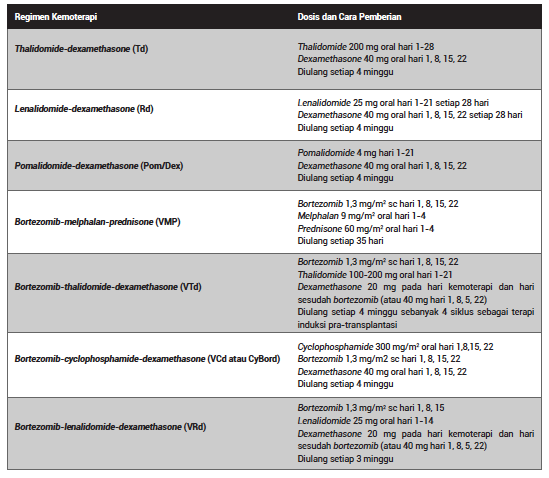
Tabel 6. Kombinasi Regimen Kemoterapi untuk MM15
9.1.3 Bortezomib
Tulisan ini akan membahas terapi bortezomib lebih mendalam, karena terapi ini tersedia di Indonesia dan studi menunjukkan bahwa bortezomib menghasilkan respons terapi yang baik sebagai terapi awal pasien MM yang baru terdiagnosis. Bortezomib adalah suatu proteasome inhibitor yang bekerja dengan menargetkan proteasome 26S, kompleks proteinase multikatalitik yang terlibat dalam degradasi protein intraseluler. Bortezomib menghambat aktivasi faktor transkripsi NF-κB dengan melindungi inhibitor I-kappa B (IκB) dari degradasi oleh proteasome 26S. Degradasi I-κB oleh proteasome mengaktifkan NF-κB, yang mengatur transkripsi protein yang berperan dalam meningkatkan kelangsungan hidup dan pertumbuhan sel, menurunkan kerentanan terhadap apoptosis, memengaruhi ekspresi molekul adhesi, dan menginduksi resistansi obat dalam sel myeloma. Bortezomib tidak hanya menargetkan sel myeloma, tetapi juga bekerja di lingkungan mikro sumsum tulang dengan menghambat pengikatan sel myeloma ke sel stroma sumsum tulang dan angiogenesis yang dipicu oleh sumsum tulang.21
Dosis awal bortezomib yang direkomendasikan adalah 1,3 mg/m2 yang diberikan sebagai injeksi bolus intravena atau subkutan selama 3-5 detik pada hari ke-1, 4, 8, dan 11 dari siklus 21 hari atau hari ke-1, 8, 15, 22 dari siklus 28 hari. gangguan dan modifikasi dosis dianjurkan untuk pasien yang mengalami toksisitas hematologi dan non hematologi tingkat 3 atau 4. Modifikasi dosis eksplisit, dimulai dengan toksisitas tingkat 1 atau 2, direkomendasikan untuk pasien yang mengalami neuropati perifer atau motorik atau nyeri neuropatik.
Pengurangan dosis menjadi 1 mg/m2 atau bahkan 0,7 mg/m2 mungkin diperlukan karena toksisitas. Bortezomib mengalami metabolisme di hati terutama melalui enzim sitokrom P450 3A4, 2C19, dan 1A2. Tidak ada studi interaksi obat formal yang telah dilakukan dengan bortezomib. Bortezomib telah dipelajari pada pasien dengan berbagai derajat gangguan ginjal, termasuk pasien yang membutuhkan dialisis. Farmakokinetik bortezomib tampaknya tidak dipengaruhi oleh derajat gangguan ginjal. Dialisis dapat mengurangi konsentrasi bortezomib; jadi bortezomib harus diberikan setelah dialisis. Bortezomib memberikan respons yang cepat dan dapat diamati dalam 2 siklus terapi.21
Efek samping paling umum yang terkait dengan bortezomib adalah gangguan gastrointestinal, trombositopenia, dan neuropati perifer. Pasien mungkin memerlukan obat antiemetik dan antidiare atau penggantian cairan karena tingginya insiden mual dan diare. Trombositopenia derajat 3 atau 4 terjadi pada lebih dari 30% pasien dan telah ditemukan bersifat sementara dan siklis. Jumlah trombosit menurun dan pulih secara terprediksi pada setiap siklus pengobatan tanpa bukti toksisitas kumulatif. Jumlah trombosit awal sebelum terapi bortezomib merupakan prediktor terjadinya trombositopenia berat. Pasien dengan jumlah trombosit baseline kurang dari 70.000/ ml telah terbukti berisiko lebih tinggi untuk trombositopenia kelas 3 atau 4. Neuropati perifer terjadi pada 37% pasien yang menjalani terapi bortezomib. Neuropati perifer derajat 3 atau 4 terjadi pada 11% pasien. Insiden neuropati perifer tampaknya tidak dipengaruhi oleh neuropati awal atau terapi sebelumnya dengan agen neurotoksik. Toksisitas tingkat 3 atau 4 lain yang dilaporkan mencakup fatigue (16%), neutropenia (14%), dan anemia (12%). Efek samping umum lainnya termasuk demam, edema, batuk, dan sakit kepala.21
Peran bortezomib dalam pengobatan MM telah berkembang sejak obat tersebut diperkenalkan ke pasaran. Kombinasi berbasis bortezomib pada kasus MM yang baru didiagnosis telah menghasilkan angka complete response/CR dan overall response yang tinggi. Selain itu, tidak tampak adanya dampak negatif pada pengambilan atau pencangkokan sel punca pada pasien yang menerima bortezomib sebagai bagian dari regimen induksi.21
Bortezomib pada awalnya dilaporkan sebagai penghambat jalur NF-κB, yang memainkan peran penting dalam patogenesis multiple myeloma (MM). Aktivitas NF-κB sel MM dimediasi melalui dua jalur yang dapat dibedakan, kanonik dan nonkanonik, yang menunjukkan aksi berlawanan setelah pengobatan bortezomib dalam sel MM. Studi terbaru tentang penghambatan proteasome dalam sel MM mengungkapkan bahwa akumulasi protein yang tidak terlipat dalam endoplasmic reticulum (ER), yang disebut dengan stres ER, dapat memicu beberapa faktor proapoptosis dan stres sel seperti akumulasi reactive oxygen species (ROS), yang dianggap menjadi mekanisme utama aksi apoptosis yang diinduksi oleh bortezomib. Beberapa faktor yang berhubungan dengan stres ER dan unfolded protein response (UPR), telah diidentifikasi dengan sensitivitas pengobatan bortezomib.Rendahnya tingkatXBP1,ATF3, danATF4, yang mengatur apoptosis yang diinduksi stres UPR dan ER, telah diamati pada responden yang buruk terhadap pengobatan bortezomib, sedangkan tiga gen lain, KLF9, Nampt, dan CDK5, dikaitkan dengan respons yang lebih baik terhadap bortezomib. Temuan ini berkontribusi pada pemahaman yang lebih baik tentang mekanisme apoptosis yang diinduksi oleh bortezomib dalam sel MM, dan studi lebih lanjut diperlukan untuk mengembangkan biomarker prediktif potensial dari kemanjuran terapi yang mengandung bortezomib. 22
Pada suatu penelitian yang semua pasiennya menerima terapi BTD (bortezomib, thalidomide, dexamethasone) sebagai terapi induksi dengan median time 5 siklus (range 2-8) didapatkan hasil bahwa pada kelompok satu (n=42) dengan nilai Scr <2 mg/dl, 8 pasien (19.0%) memperoleh complete response/CR, 14 (33.3%) very good partial response/VGPR, 12 (28,6%) partial response/PR dan overall response rate/ORR 81,0%. Pada kelompok kedua (n=30) dengan nilai Scr ≥2 mg/dl, 6 pasien (20,0%) memperoleh CR, 8 (26,7%) VGPR, 10 (33,3%) PR dan ORR 80,0%. Tidak ada perbedaan bermakna antara kedua kelompok (p>0.05). Pada kelompok kedua, 33,3% mengalami perbaikan fungsi ginjal menjadi normal dan 46,7% mengalami perbaikan nilai laju filgrasiglomerulus. Median waktu untuk terjadinya perbaikan fungsi ginjal ini adalah 1,4 bulan. Dari 12 pasien yang menjalani hemodialisis pada saat diagnosis MM, 8 pasien tidak perlu lagi menjalani dialisis setelah 4 siklus terapi.23
Dalam studi fase 2 oleh Ludwid, et al. (2010) tampak bahwa regimen BDD (bortezomib, doxorubicin, dexamethasone) mampu membantu memperbaiki kerusakan ginjal akut yang diinduksi oleh light chain. Efek samping hematologi yang paling sering dijumpai adalah anemia, neutropenia, dan trombositopenia, sementara efek samping nonhematologi yang paling sering dijumpai adalah infeksi, fatigue, dan polineuropati.
Bortezomib adalah suatu proteasome inhibitor yang memiliki aktivitas antimyeloma yang kuat dan dapat membantu memperbaiki fungsi ginjal dengan mengurangi toksisitas monoclonal light chain dan menekan NF-κb dalam sel tubulus sehingga memperbaiki respons inflamasi. Serum cystatin-C juga dilaporkan mengalami perbaikan setelah terapi bortezomib bortezomib pada pasien dengan atau tanpa gangguan fungsi ginjal adalah sama. Hal ini dapat disebabkan karena farmakokinetik bortezomib tidak dipengaruhi oleh derajat fungsi ginjal, dan oleh karena itu, bortezomib tidak memerlukan penyesuaian dosis pada pasien dengan gangguan ginjal.23
Berdasarkan hasil dari berbagai penelitian, dapat disimpulkan bahwa regimen berbasis bortezomib merupakan regimen yang terbukti multiple myeloma (MM), termasuk jika disertai dengan gangguan ginjal. Regimen VTD dapat menjadi pilihan lini pertama pada pasien MM dengan gangguan ginjal karena dapat membantu memperbaiki prognosis pasien sebaik pada kasus MM tanpa gangguan ginjal.23,24,25
9.1.4 Autologous Stem Cell Transplant (ASCT)
Tata laksana multiple myeloma (MM) dengan autologous peripheral blood stem cell transplant (PBSCT) atau autologous stem cell transplant (ASCT) bukanlah hal yang baru di dunia karena telah mulai diperkenalkan sejak tahun 1980-an, namun di Indonesia, tindakan ini masih terbilang sangat baru. Beberapa wilayah di dunia tidak memiliki akses terhadap transplantasi sel punca, terutama sub-Sahara Afrika (kecuali Afrika Selatan).2
Terapi melphalan dosis tinggi diikuti oleh transplantasi sel punca autologus (HDT/ASCT) pada pasien dengan multiple myeloma pernah menjadi terapi standar selama 20 tahun hingga akhirnya agen-agen terapi yang baru (immunomodulatory drugs/IMIDs dan proteasome inhibitor) diperkenalkan. Sejak terapi modern digunakan, para peneliti mengevaluasi kembali efikasi dari HDT/ASCT pada kasus MM.
Hasil metaanalisis yang mengevaluasi studi-studi fase 3 yang membandingkan HDT/ASCT dengan standard-dose therapy (SDT) menggunakan agen-agen terapi yang baru, serta studi yang membandingkan HDT/ASCT dengan konsolidasi bortezomib, lenalidomide, dan dexamethasone serta tandem transplantation menunjukkan bahwa HDT/ASCT berasosiasi dengan PFS yang lebih baik dengan efek toksisitas yang minimal. Tandem HDT/ASCT dan single HDT/ASCT dengan konsolidasi bortezomib, lenalidomide, dan dexamethasone terbukti superior dibandingkan single HDT/ASCT and SDT dalam hal PFS. Diperlukan follow-up yang lebih panjang untuk melihat pengaruh regimen ini terhadap OS.26
Pada pasien MM, ASCT meningkatkan progression-free survival (PFS) dan overall survival (OS) dibandingkan dengan kemoterapi saja. Saat ini, Amerika Serikat melakukan sekitar 10.000 ASCT per tahun dengan metode peripheral blood stem cell transplant (PBSCT).5 Di Indonesia ASCT dengan metode PBSCT juga sudah dapat dilakukan di beberapa center. Di Surabaya (FK Unair-RSUD Dr. Soetomo-RS Unair) telah dilakukan 14 kali ASCT dengan metode PBSCT sejak tahun 2014.
ASCT meningkatkan median OS pada pasien MM sekitar 12 bulan. Uji coba secara acak menemukan OS yang serupa dengan ASCT dini (segera setelah empat siklus terapi induksi) dibandingkan ASCT yang tertunda (pada saat kambuh, sebagai terapi penyelamatan). Penelitian oleh Intergroupe Francophone du Myelome (IFM) membandingkan ASCT dini dan tertunda pada pasien yang diobati dengan VRd diikuti dengan pemeliharaan lenalidomide. Pasien diacak untuk menerima VRd (tiga siklus) diikuti oleh ASCT dan kemudian konsolidasi VRd (dua siklus) dibandingkan dengan delapan siklus VRd dengan ASCT yang disediakan jika terjadi relapse. Kedua kelompok menerima perawatan lenalidomide selama 1 tahun. Peningkatan yang signifikan dalam PFS terlihat seperti yang diharapkan dengan ASCT awal, tetapi sejauh ini belum diterjemahkan ke dalam perbedaan OS. Berdasarkan hasil ini, masuk akal untuk mempertimbangkan ASCT tertunda pada pasien dengan MM risiko standar yang lebih memilih pendekatan semacam itu karena alasan pribadi dan logistik.15
9.2 Terapi suportif simtomatik untuk mencegah morbiditas dari komplikasi yang ditimbulkan oleh MM
Terapi suportif pasien MM meliputi terapi dini terhadap infeksi, mengendalikan hiperkalsemia dengan glucocorticoid, hidrasi, dan natriuresis.19 Pemberian bisphosphonate dalam jangka panjang dapat mengurangi kerusakan skeletal.27 Nefropati akibat hiperurisemia dan dehidrasi harus dihindari untuk mencegah terjadinya gagal ginjal.7
DAFTAR PUSTAKA