Dislipidemia Aterogenik pada Pasien Diabetes Melitus Tipe 2 Patofisiologi dan Pilihan Terapi
Rulli Rosandi
Rulli Rosandi

Dislipidemia Aterogenik pada Pasien Diabetes Melitus Tipe 2 Patofisiologi dan Pilihan Terapi
Sumber: Medicinus April 2021 vol. 34 issue 1
Rulli Rosandi
Divisi Endokrin Metabolik dan Diabetes RSU Dr. Saiful Anwar – Fakultas Kedokteran Universitas Brawijaya Malang
Abstrak
Dislipidemia aterogenik mempunyai karakteristik berupa peningkatan kadar trigliserida dan small dense low-density lipoprotein (sdLDL), serta penurunan kadar high-density lipoprotein (HDL). Kondisi ini disertai dengan peningkatan kadar dari very-low-density lipoprotein yang kaya akan trigliserida, apolipoprotein B, dan oxidized low-density lipoprotein (oxLDL). Profil lipid ini mempunyai peranan penting di dalam patogenesis gangguan kardiovaskular seperti penyakit jantung koroner, peripheral artery disease, dan stroke. Diabetes melitus adalah faktor risiko independen untuk terjadinya aterosklerosis prematur. Statin intensitas tinggi dan sedang (moderate) masih merupakan pilihan terapi yang direkomendasikan dalam tata laksana kelainan ini. Saat ini juga makin berkembang alternatif terapi di luar statin yang perannya masih mendampingi pemberian statin. Ezetimibe dan proprotein convertase subtilisin/kexin type 9 (PCSK9) inhibitor mulai banyak disebutkan dalam panduan penatalaksanaan dislipidemia terkini, selain tetap mengedepankan pendekatan nonfarmakologis seperti pengaturan diet dan latihan fisik.
Abstract
Atherogenic dyslipidemia is characterized by increase in triglyceride and small dense lipoprotein (sdLDL) level, also decrease in high-density lipoprotein (HDL) level. This condition is accompanied by increased TG-rich very-low-density lipoprotein, apolipoprotein B, and oxidized low-density lipoprotein (oxLDL). This lipid profile plays an important role in the pathogenesis of cardiovascular disorders such as coronary heart disease, peripheral artery disease, and stroke. Diabetes mellitus is an independent risk factor for premature atherosclerosis. High- and moderate-intensity statins are recommended therapeutic options in the management of this disorder. Currently, there are also some therapeutic options other than statin to accompany statin therapy. Ezetimibe and proprotein convertase subtilisin/kexin type 9 (PCSK9) inhibitor are mentioned a lot in current lipid management guidelines in addition to nonpharmacologic approach such as diet and physical exercise.
Pendahuluan
Di seluruh dunia, tidak kurang dari 463 juta individu berusia 20-79 tahun termasuk ke dalam kelompok orang dengan diabetes melitus atau yang biasa disebut dengan diabetisi. Jumlah ini diperkirakan akan terus meningkat, sehingga diproyeksikan akan mencapai 700 juta orang pada tahun 2045.1 Data dari International Diabetes Federation (IDF) menunjukkan bahwa terdapat 10,7 juta diabetisi di Indonesia, yang diproyeksikan akan meningkat menjadi 13,7 juta orang pada tahun 2030.1 Makin meningkatnya jumlah individu dengan diabetes ini merupakan tantangan sekaligus ancaman terhadap layanan kesehatan dan status sosioekonomi. Diabetisi memiliki risiko untuk mengalami komplikasi terkait diabetes yang berpotensi serius dan mengancam jiwa, sekaligus mengakibatkan peningkatan biaya kesehatan, mengurangi kualitas hidup, serta memberikan tekanan psikologis tersendiri bagi pasien dan keluarganya. Berbagai komplikasi ini jika tidak ditangani dengan baik maka akan meningkatkan frekuensi admisi rumah sakit dan juga risiko kematian. Pada tahun 2010, tercatat sekitar 3,96 juta kematian terkait diabetes melitus dengan angka yang meningkat di tahun 2015 menjadi 5 juta kematian, di mana jumlah tersebut lebih kurang sama dengan 1 kematian setiap 6 detik.2 Sebagian besar pasien diabetes memiliki sedikitnya satu komplikasi terkait diabetes, dan komplikasi kardiovaskular masih menjadi penyebab kematian utama pada pasien diabetes melitus. Pada pasien diabetes melitus tipe 2 (DMT2), penyakit kardiovaskular terjadi 14,6 tahun lebih awal, dan dalam derajat yang lebih berat jika dibandingkan dengan individu tanpa diabetes. Lebih jauh lagi, data menunjukkan bahwa pasien DMT2 memiliki kemungkinan untuk mengalami komplikasi kardiovaskular dua kali lebih besar dibandingkan pasien nondiabetes terlepas dari faktor usia, riwayat merokok, indeks massa tubuh (IMT), dan tekanan darah sistolik. Diabetes juga berhubungan dengan risiko kematian dikarenakan penyakit kardiovaskular dua kali lipat lebih besar.3 Peningkatan risiko penyakit kardiovaskular pada pasien diabetes melitus salah satunya disebabkan oleh dislipidemia aterogenik.4 Tulisan ini bertujuan untuk membahas patofisiologi dan pilihan terapi pada kasus dislipidemia aterogenik dalam hubungannya dengan penyakit diabetes melitus, terutama DMT2.
Definisi dan Epidemiologi
Dislipidemia aterogenik (DA) merupakan suatu kondisi yang ditandai dengan peningkatan kadar trigliserida (TG) dan small dense low-density lipoprotein (sdLDL), serta penurunan kadar high-density lipoprotein (HDL). Kondisi ini disertai dengan peningkatan kadar dari very-low-density lipoprotein yang kaya akan trigliserida, apolipoprotein B, dan oxidized low-density (oxLDL).5 Kondisi klinis ini pada awal mulanya diperkenalkan oleh Austin dan koleganya pada tahun 1990, di mana kondisi ini sering dijumpai pada individu dengan diabetes melitus, sindrom metabolik, obesitas dan resistansi insulin. Oleh karenanya, dislipidemia aterogenik ini juga seringkali dikenal dengan istilah dislipidemia diabetes atau dislipidemia sindrom metabolik, yang sekaligus merupakan faktor risiko kardiovaskular untuk individu dengan kondisi ini.5 Data dari Tiongkok menunjukkan prevalensi dislipidemia pada pasien DMT2 ditemukan cukup tinggi yaitu sekitar 59,3%,6 sedangkan data dari Bangladesh menunjukkan prevalensi dislipidemia pada pasien DMT2 laki-laki sebesar 73%, dan pada perempuan sebesar 71%.7 Di Indonesia, data Riset Kesehatan Dasar (Riskesdas) tahun 2013 menunjukkan terdapat 35,9% penduduk Indonesia dengan kadar kolesterol di atas normal. Soebardi dkk. menunjukkan prevalensi hiperkolesterolemia, hipertrigliseridemia, kolesterol HDL yang rendah, dan kadar kolesterol LDL yang tinggi pada pasien DMT2 di Indonesia secara berurutan adalah sebesar 67,7%; 54,9%; 36,8%; dan 91,7%.8 Studi ini juga menemukan bahwa kadar trigliserida yang tinggi dan HDL yang rendah lebih banyak dijumpai pada populasi diabetes melitus tipe 2 dibandingkan dengan populasi prediabetes.
Patofisiologi
Secara umum, patofisiologi dari dislipidemia aterogenik ini bersifat kompleks dan banyak hal yang masih belum dipahami sepenuhnya. Kondisi hipertrigliseridemia, kadar kolesterol HDL yang rendah, dan sdLDL yang tinggi dapat dijumpai sebelum diagnosis DMT2 ditegakkan, sehingga hiperglikemia saja tidak mampu untuk menjelaskan secara utuh perubahan parameter lipid pada dislipidemia aterogenik. Sejauh ini patofisiologi awal yang dipahami pada pasien diabetes melitus tipe 2 adalah terjadinya resistansi insulin.9 Resistansi insulin didefinisikan sebagai respons abnormal dari jaringan terhadap insulin, baik insulin endogen maupun insulin eksogen.10 Hipertrigliseridemia diduga sebagai abnormalitas lipid yang paling dominan pada kondisi resistansi insulin, sehingga merupakan karakteristik profil lipid dari kondisi dislipidemia aterogenik.
Pada metabolisme lipid, fungsi dari insulin adalah untuk menghambat pelepasan free fatty acid (FFA). Dengan adanya resistansi insulin, maka fungsi supresi ini hilang, yang berakibat pada peningkatan pelepasan FFA ke dalam sirkulasi. Peningkatan ini akan ditransportasikan ke liver dan otot melalui aliran darah. Meningkatnya FFA di liver menyebabkan liver terstimulasi untuk memproduksi dan melepaskan very-low-density lipoprotein (VLDL). Peningkatan produksi VLDL yang merupakan transporter utama trigliserida merupakan gambaran adanya resistansi insulin. Insulin mempunyai peran yang sangat besar dalam semua tahapan produksi dan sekresi VLDL.11 Di liver, insulin menghambat proses transkripsi microsomal triglyceride transfer protein (MTP) yang berperan dalam transfer trigliserida pada nascent apolipoprotein B (apoB), yang merupakan protein permukaan utama dari VLDL. Kecepatan produksi dari apoB relatif konstan, sehingga jika terjadi peningkatan produksi FFA akan menyebabkan peningkatan produksi VLDL. Ada dua tipe VLDL yang disintesis, yang pertama adalah VLDL-1 yang kaya akan trigliserida (TG) dan yang kedua adalah VLDL-2 yang lebih sedikit konsenterasi TG-nya. VLDL1 memiliki kandungan trigliserida yang tinggi disertai kadar apolipoprotein CIII (apo CIII) dan apolipoprotein E yang juga tinggi. VLDL-1 merupakan parameter gambaran konsentrasi plasma trigliserida dan dikatakan berkaitan erat dengan sensitivitas insulin, sebagaimana perhitungan yang dilakukan dengan HOMAIR.11 Produksi VLDL-1 jauh lebih banyak dibandingkan dengan produksi VLDL-2. Produksi VLDL-1 ini terdiri dari 3 langkah yaitu lipidasi atau penambahan molekul hidrofobik pada ApoB100 di hepatosit sehingga terbentuk nascent pre-VLDL. Langkah kedua yaitu nascent pre-VLDL ini kemudian akan mengalami lipidasi kembali sehingga membentuk partikel VLDL-2. Langkah terakhir adalah proses lipidasi dari VLDL-2 untuk membentuk VLDL-1. Dalam tahapan selanjutnya, adalah perubahan dari VLDL-1 yang kaya akan trigliserida ini menjadi bentuk kolesterol LDL yang kecil dan padat (small dense LDL/sdLDL) melalui dua tahapan. Tahap pertama berupa transfer TG dari VLDL-1 menjadi LDL oleh enzim cholesteryl ester transfer protein (CETP) yang dilanjutkan dengan tahap kedua yaitu konversi LDL yang kaya akan TG ke sdLDL dengan bantuan enzim hepatic lipase (HL).
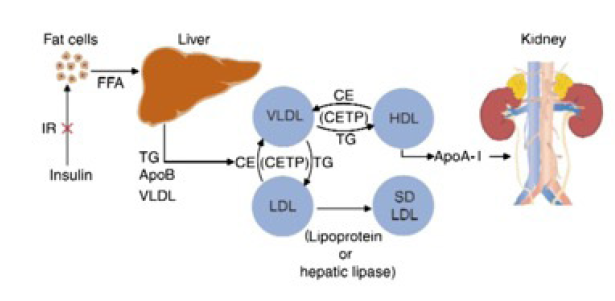
Gambar 1. Patogenesis dislipidemia aterogenik. Resistansi insulin mengakibatkan peningkatan lipolisis yang berdampak pada peningkatan free fatty acid. Selanjutnya akan terjadi rangkaian proses yang menyebabkan peningkatan trigliserida dan small dense LDL serta penurunan HDL.13 (IR: insulin resistance; TG: trigliserida; VLDL: very-low-density lipoprotein; CE: cholesteryl ester; CETP: cholesteryl ester transport protein; ApoB: apolipoprotein B; FFA: free fatty acid; LDL: low-density lipoprotein; HDL: high-density lipoprotein; ApoA: apolipoprotein A)
Small dense LDL lebih berbahaya dibandingkan dengan LDL karena kemampuan penetrasinya yang lebih tinggi pada tunika arterial intima pembuluh darah dan juga kemampuannya untuk mengendap pada pembuluh darah yang lebih besar. Hal ini dimungkinkan karena kecenderungan untuk berikatan dengan proteoglikan arteri pada matriks ekstraseluler yang lebih besar dibandingkan dengan LDL.5 Lebih lanjut dikatakan bahwa ikatan tidak langsung melalui bridging molecules seperti lipoprotein lipase dan decorin akan mengakibatkan retensi atau pengendapan ini menjadi lebih kuat. Partikel sdLDL yang mengendap di tunika intima ini kemudian akan mengalami modifikasi dengan adanya stres oksidatif. Proses oksidasi LDL di tunika intima ini berikutnya akan memicu rangkaian proses yang berujung kepada terbentuknya makrofag sel busa dan pembentukan plak. Studi lain menyebutkan bahwa sdLDL juga mengganggu respons vasodilatasi endotel pembuluh darah yang difasilitasi oleh acetylcholine yang akan mengganggu fungsi vaskular pada pasien dengan DMT2.12 Di sirkulasi, sdLDL memiliki afinitas yang rendah terhadap reseptor kolesterol LDL yang ada di hepatosit, sehingga menyebabkan rendahnya ambilan dan bersihan sdLDL yang berdampak pada peningkatan jumlahnya di sirkulasi. Selain itu, VLDL yang tinggi juga akan menyebabkan pertukaran dari kolesterol ester baik dari HDL maupun LDL untuk VLDL-TG. ApoA-I ini kemudian akan terpisah dari TG-enriched HDL. ApoA-I yang sudah terpisah ini kemudian akan dikeluarkan dari plasma untuk kemudian diekskresikan melalui ginjal, sehingga mengurangi jumlah HDL yang diperlukan untuk reverse cholesterol transport. TG-enriched LDL kemudian akan mengalami lipolisis menjadi lebih kecil dan padat. Hal inilah yang menyebabkan berkurangnya kadar HDL dan meningkatnya jumlah dari small dense LDL.13
Kondisi hipertrigliseridemia pada dislipidemia aterogenik, selain disebabkan oleh produksi VLDL yang meningkat, juga dimungkinkan karena berkurangnya kecepatan bersihan akibat penurunan kinerja enzim lipoprotein lipase. Kondisi ini disebabkan oleh lepasnya enzim ini dari permukaan endotel sebagai akibat dari peningkatan kadar FFA. Peningkatan konsentrasi glukosa darah juga akan menyebabkan meningkatnya produksi VLDL. Hal ini dikarenakan kondisi glukosa darah yang tinggi disertai dengan kadar insulin yang rendah akan menyebabkan peningkatan ekspresi ApoCIII yang merupakan protein permukaan dari apoB dan HDL, yang kemudian menghambat kerja dari enzim lipoprotein lipase. 11
Tata Laksana
1.1. Screening dan pemeriksaan laboratorium
Melihat besarnya masalah yang ditimbulkan dari dislipidemia aterogenik, terutama dalam hubungannya dengan risiko komplikasi kardiovaskular, panduan tata laksana diabetes melitus memasukkan rekomendasi screening untuk risiko kardiovaskular ini. Panduan tata laksana dislipidemia yang dikeluarkan oleh PB Perkeni tahun 2019 menyebutkan beberapa sistem screening yang dapat digunakan seperti skor risiko Framingham yang populer karena praktis digunakan, serta pooled cohort equation, systematic coronary risk evaluation (SCORE), Q-risk, Reynold, PROCAM, COURE, Globorisk, juga United Kingdom Prospective Diabetes Study (UKPDS).14 Devaraj merekomendasikan beberapa pemeriksaan yang bisa dilakukan untuk melakukan assessment dislipidemia pada pasien diabetes.15

Tabel 1. Evaluasi laboratorium dislipidemia pada pasien DMT2
1.2. Terapi nonfarmakologis
Berdasarkan patofisiologi dislipidemia aterogenik yang relatif kompleks, maka dapat dipahami tata laksananya yang bersifat multimodalitas. Fondasi paling utama terletak pada terapi nonfarmakologis berupa pengaturan diet serta aktivitas dan latihan fisik. Di bagian awal telah disebutkan bahwa resistansi insulin merupakan pintu masuk secara patofisiologi untuk dislipidemia aterogenik sehingga penurunan berat badan menjadi suatu keniscayaan dalam tata laksana ini. Penurunan berat badan sekitar 5% dari berat badan awal dikatakan dapat memperbaiki sensitivitas insulin, kendali glukosa darah, dan profil lipid.16 Penurunan berat badan juga dihubungkan dengan peningkatan kadar HDL dan penurunan kadar trigliserida. Diet tinggi karbohidrat berperan besar dalam peningkatan kadar TG pada dislipidemia aterogenik. Pembatasan asupan karbohidrat akan memperbaiki profil lipid aterogenik walaupun belum tercapai penurunan berat badan yang diinginkan, berbeda dengan diet rendah lemak yang membutuhkan penurunan berat badan untuk perbaikan profil lipid aterogenik.5 Selain karbohidrat, peningkatan asupan serat sebanyak 5-10 gram/hari dapat menurunkan kadar LDL sekitar 3-5%, asupan plant stanol ester seperti yang banyak terkandung dalam sereal, kacang-kacangan, sayur dan buah-buahan sebanyak 2 gram/hari juga diketahui dapat menurunkan kadar LDL sebanyak 6-15%.
Peningkatan aktivitas dan latihan fisik serta pengaturan berat badan juga memberikan perbaikan pada dislipidemia aterogenik. Aktivitas dan latihan fisik secara rutin selama sekitar 12 minggu dapat meningkatkan HDL sebesar 4-22% dari kadar awal. Selain itu, latihan fisik yang dilakukan sekitar 1 jam per hari dalam 5-7 hari secara rutin dapat membantu menurunkan berat badan.5
Parameter metabolik di satu sisi menunjukkan perbaikan dengan pengaturan diet dan peningkatan rutinitas aktivitas dan latihan fisik, namun di sisi lain belum bisa dikorelasikan secara langsung dengan penurunan risiko kardiovaskular sebagaimana yang disimpulkan dari studi Action for Health in Diabetes (The Look AHEAD) yang pada kesimpulannya menuliskan bahwa penurunan berat badan jangka panjang melalui intervensi gaya hidup meskipun terlihat memperbaiki sebagian besar faktor risiko kardiovaskular, namun belum terlihat menurunkan risiko kardiovaskular itu sendiri secara bermakna.17 Dengan demikian pada kebanyakan kasus dibutuhkan kombinasi antara modifikasi gaya hidup dengan pendekatan farmakologis. Penurunan glukosa darah merupakan faktor yang sangat penting untuk dilakukan karena kontrol glukosa darah yang buruk akan memperparah abnormalitas lipid, terutama hipertrigliseridemia.
1.3. Terapi farmakologis
Pedoman pengelolaan dislipidemia Perkeni 2019 menjelaskan prinsip dasar dalam terapi farmakologis untuk dislipidemia yakni untuk menurunkan risiko penyakit kardiovaskular. Terdapat beberapa golongan obat hipolipidemik yang dapat digunakan, yaitu:
a. Statin
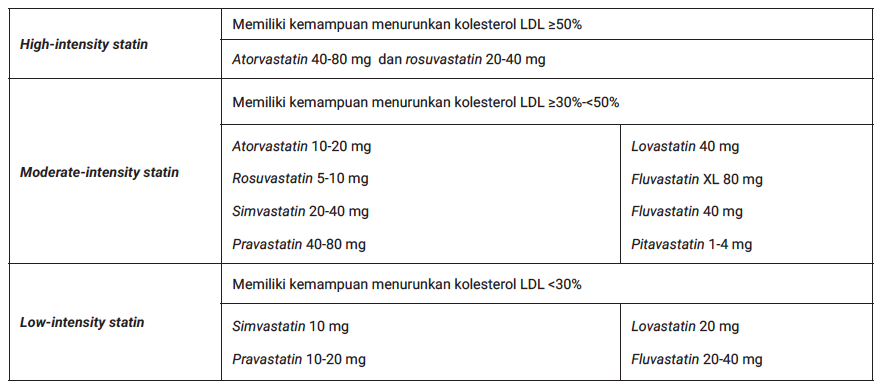
Statin bekerja dengan menghambat enzim 3-hydroxy-3-methylglutaryl coenzyme A reductase (HMG-CoA reductase) sehingga dapat menyebabkan penurunan kadar kolesterol LDL yang beredar sebesar 30-50% dari baseline tergantung kepada jenis statin yang digunakan, dosis, farmakogenenetik, dan kepatuhan pasien. Dalam 20 tahun terakhir terdapat banyak studi yang berfokus pada pencegahan primer dan sekunder dengan terapi menggunakan obat golongan statin, terutama pada pasien diabetes melitus tipe 2. Sebuah metaanalisis dari 14 randomized controlled trials yang dilakukan oleh The Cholesterol Treatment Trialists Collaboration melakukan evaluasi pada 18.686 pasien diabetes (terdiri dari 1.466 pasien diabetes melitus tipe 1 dan 17.220 pasien diabetes melitus tipe 2) yang mendapatkan statin rerata selama 4,3 tahun. Hasil metaanalisis ini menyimpulkan setiap penurunan 40 mg/dl kadar kolesterol LDL akan didapatkan penurunan all-cause mortality sebesar 9% dan penurunan kematian karena jantung koroner atau infark miokardium, revaskularisasi koroner dan stroke sebesar 21%.18 Meskipun mekanisme kerja statin lebih mengarah pada penurunan kadar kolesterol LDL melalui upregulating reseptor LDL, namun bukti ilmiah juga menunjukkan bahwa statin dapat menurunkan apoB100 dan sdLDL yang merupakan dua faktor risiko utama dislipidemia aterogenik.19 Berdasarkan hal tersebut, hampir semua panduan tata laksana dislipidemia memasukkan statin sebagai terapi yang diindikasikan pada pasien diabetes melitus. Berdasarkan kemampuannya dalam menurunkan kolesterol LDL, statin dibedakan menjadi tiga kelompok, yaitu:14
b. Ezetimibe
Ezetimibe merupakan obat yang bekerja menurunkan kadar kolesterol dengan cara menghambat absorpsi kolesterol melalui inhibisi Niemann-Pick C1-like protein 1 (NPC1L1) yang berada di bagian lumen duodenum dan jejunum. Pedoman Perkeni 2019, mempertimbangkan pemberian obat golongan ini pada pasien yang tidak menoleransi pemberian statin selain penggunaan untuk mendampingi pemberian statin agar didapatkan penurunan kolesterol LDL yang lebih besar.14 Pemberian ezetimibe efektif dalam menurunkan kolesterol LDL terutama jika dikombinasi dengan pemberian statin. Manfaat ini ditunjukkan pada hasil studi IMProved Reduction of Outcomes: Vytorin Efficacy International Trial (IMPROVE-IT) yang melibatkan 18.144 pasien dengan sindrom koroner akut (SKA), di mana dijumpai dengan hasil penurunan kolesterol LDL sebesar dari 70-55 mg/dl setelah terapi menggunakan kombinasi ezetimibe dan statin selama 7 tahun diperoleh penurunan major adverse cardiovascular event (MACEs) setidaknya sebesar 7%. Subgroup analysis memperlihatkan kombinasi ezetimibe dan statin lebih signifikan untuk hasil yang positif apabila diberikan pada pasien diabetes, di mana MACE bisa dikurangi sebesar 14% (Hazard Ratio [HR] 0,860; 95% confidence interval [CI] 0,78-0,94) pada pasien dislipidemia dengan diabetes dibandingkan dengan penurunan nonsignifikan sebesar 2% (HR 0.98; 95% [CI] 0,92-1,04) pada pasien tanpa diabetes melitus. Penjelasan untuk hal ini masih dalam perdebatan, namun diduga fokus utama adalah dengan mengurangi komponen non-LDL pada kondisi dislipidemia aterogenik.
c. Bile Acid Sequestrant
Resin asam empedu atau bile acid sequestrant mempunyai efek hipolipidemik melalui kerja pada lumen ileum terminalis, berbeda dengan ezetimibe yang berkerja pada lumen pada duodenum dan jejunum. Bile acid atau asam empedu diproduksi di liver dari kolesterol dan kemudian dikeluarkan melalui lumen usus, namun sebagian besar asam empedu diabsorpsi kembali melalui ileum terminalis ke liver. Obat golongan ini mengikat asam empedu dan mencegah reabsorpsi kolesterol ke dalam darah sehingga asam empedu dapat dikeluarkan dari sirkulasi enterohepatik. Dengan kondisi ini, liver yang berkurang empedunya akan melakukan sintesis asam empedu kembali dengan bahan dasar kolesterol, yang akan menurunkan jumlah kolesterol LDL di sirkulasi. Obat golongan ini sudah lama diketahui mempunyai potensi dalam menurunkan kolesterol, namun belum ada studi yang dilakukan untuk populasi dislipidemia aterogenik. Studi dari Lipid Research Clinics Coronary Primary Prevention Trial menunjukkan penurunan kolesterol dengan pemberian obat ini dapat menurunkan major adverse cardiovascular event (MACE) sebesar 20%, namun dalam studi ini tidak dilibatkan individu dengan diabetes melitus.20
d. Fibrate
Setidaknya terdapat lima jenis obat dari golongan fibrate yang diketahui memberikan manfaat klinis yaitu clofibrate, bezafibrate, ciprofibrate, gemfibrozil, dan fenofibrate. Di Indonesia saat ini yang banyak beredar adalah gemfibrozil dan fenofibrate. 14 Mekanisme kerja obat golongan ini dalam tata laksana dislipidemia adalah melalui interaksi dengan peroxisome proliferator-activated receptor α (PPAR-α) yang kemudian akan memengaruhi target gen yang berperan dalam transpor dan metabolisme lipid terutama di jaringan liver dan lemak serta di otot, ginjal dan kardiomiosit.21 Efek utama dari terapi obat golongan fibrate tampak terutama pada penurunan kadar trigliserida sebesar 28-77%, namun juga mempunyai efek sekunder berupa peningkatan kolesterol HDL sampai dengan 20% dan penurunan kolesterol LDL sampai dengan 36%, tergantung jenis fibrate yang digunakan dan kadar lipid awal.21
Studi efikasi penggunaan fibrate dalam menurunkan morbiditas dan mortalitas kardiovaskular memberikan hasil yang bervariasi.22 Beberapa metaanalisis menyebutkan adanya penurunan kejadian kardiovaskular pada pasien dengan kadar TG yang tinggi dan kadar kolesterol HDL yang rendah, namun tidak menurunkan mortalitas terkait kardiovaskular dan mortalitas total, sehingga panduan dari European Society of Cardiology 2019 menyimpulkan bahwa data efikasi penggunaan fibrate dengan tujuan kendali risiko kardiovaskular tidak sekuat data dari statin. 22 Pemberian fibrate dapat dipertimbangkan pada pasien dengan peningkatan kadar trigliserida namun menoleransi pemberian statin. Perkeni 2019 merekomendasikan penggunaan fibrate sebagai terapi lini pertama pada pasien dengan kadar trigliserida >500 mg/dl dengan tujuan utama untuk mencegah pankreatitis. Terapi fibrate juga dapat ditambahkan sebagai kombinasi dengan statin pada pasien dengan risiko tinggi dan telah mendapatkan terapi statin, namun kadar TG masih >200 mg/dl.14
e. Proprotein convertase subtilisin/kexin type 9 inhibitor (PCSK9 inhibitor)
Proprotein convertase subtilisin/kexin type 9 (PCSK9) merupakan zimogen yang diekspresikan oleh hepatosit, yang beredar dalam plasma dan mengikat reseptor LDL bersama dengan LDL dan berperan dalam endositosis LDL yang diperantarai reseptor. Target kerja dari PCSK9 ini adalah kompleks reseptor-ligan yang berperan dalam degradasi lisosom, sehingga mengalihkan reseptor dari jalur daur ulang normalnya, yang berakibat liver mengalami penurunan kemampuan dalam membersihkan partikel LDL dari darah, sehingga terjadi peningkatan kadar LDL dalam darah. Penghambatan PCSK9 akan meningkatkan jumlah dari reseptor LDL yang berujung pada penurunan kadar LDL dalam darah. PCSK9 inhibitor dapat menurunkan kadar kolesterol LDL sekitar 60% bergantung kepada dosis yang digunakan. Pemberian bersamaan dengan statin dapat menurunkan kolesterol LDL 46-73% lebih besar dibandingkan dengan plasebo dan 30% lebih besar dibandingkan dengan ezetimibe. Perbedaan utama dari statin adalah pemberian obat kelompok ini juga akan menurunkan kadar lipoprotein Lp(a) sekitar 30-40%.
Terdapat dua studi besar yang menggunakan golongan obat ini yaitu studi Further Cardiovascular Outcomes Research With PCSK9 Inhibition in Subjects With Elevated Risk (FOURIER Trial),23 yang melihat efikasi dari evolocumab dan studi Evaluation of Cardiovascular Outcomes After an Acute Coronary Syndrome During Treatment With Alirocumab (Odyssey outcome) yang menilai efikasi dari alirocumab. 24 PCSK9 inhibitor ini dapat mengurangi risiko kardiovaskular pada pasien dengan ASCVD stabil atau recent acute coronary syndrome (ACS) yang sudah diterapi dengan moderate- dan high-intensity statin. 25
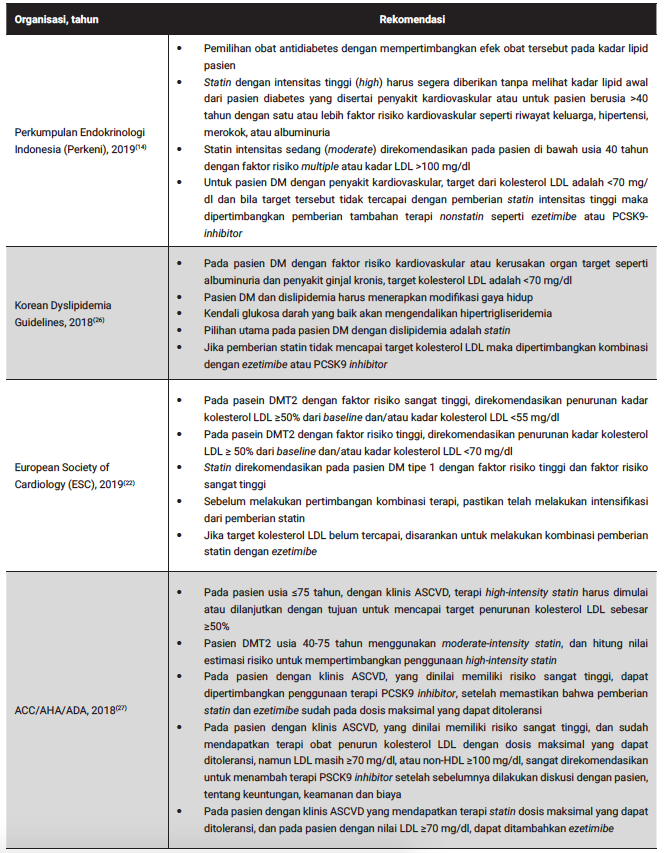
1. Panduan pengelolaan dislipidemia aterogenik Hampir semua panduan pengelolaan dislipidemia aterogenik yang dikeluarkan oleh organisasi seminat besar di dunia mengedepankan pengelolaan optimal untuk kolesterol LDL baik, dengan menggunakan baik moderate-intensity statin maupun high-intensity statin. Rangkuman panduan pengelolaan dislipidemia pada pasien diabetes melitus dapat dilihat pada tabel 2.
Tabel 2. Rangkuman rekomendasi pengelolaan dislipidemia pada pasien diabetes melitus

Kesimpulan
Dislipidemia aterogenik mempunyai karakteristik peningkatan kadar trigliserida, apoB, sdLDL dan penurunan kolesterol HDL. Kombinasi ini memberikan peningkatan risiko ASCVD yang signifikan pada pasien dengan diabetes melitus. Hingga saat ini panduan pengelolaan dislipidemia pada pasien diabetes mellitus masih mengedepankan penggunaan moderate- dan high-intensity statin untuk tata laksana dislipidemia aterogenik yang didasarkan pada risiko ASCVD dan risiko lain yang menyertai. Ezetimibe menunjukkan hasil yang positif dalam tata laksana dislipidemia pada pasien diabetes melitus, sehingga saat ini direkomendasikan sebagai pendamping pertama statin dengan pertimbangan efektivitas dan cost. PCSK9 inhibitor merupakan kelompok obat hipolipidemik yang sangat menjanjikan dengan tingkat keamanan dan efikasi telah dibuktikan, besar harapan obat golongan ini menjadi lebih terjangkau dari segi harga sehingga dapat digunakan secara luas.
DAFTAR PUSTAKA