Peran microRNA (miRNA) pada Fibrosis Hati
dr. Brilliant Van Fitof S.R., Sp.PD
dr. Brilliant Van Fitof S.R., Sp.PD
Peran microRNA (miRNA) pada Fibrosis Hati
dr. Brilliant Van Fitof S.R.
Fakultas Kedokteran Universitas Sebelas Maret/RSUD Dr. Moewardi Surakarta
Korespondensi: Brilliant Van Fitof S.R.
Fakultas Kedokteran Universitas Sebelas Maret/RSUD Dr. Moewardi Surakarta. Email: van.fitof@gmail.com
ABSTRAK
MicroRNA (miRNA atau miR) adalah kelompok RNA endogen noncoding yang terlibat dalam berbagai proses seluler yaitu perkembangan, proliferasi, diferensiasi, dan apoptosis sel, serta respons terhadap stres. Gangguan pada miRNA baik berupa mutasi, delesi, peningkatan, atau penurunan ekspresi dapat mengakibatkan berbagai penyakit. Fibrosis hati diartikan sebagai timbunan yang berlebihan dari protein fibrilar extracellular matrix (ECM), seperti kolagen I dan III di celah Disse. Penyebab umum fibrosis hati meliputi alcoholic steatohepatitis (ASH), nonalcoholic fatty liver disease (NAFLD), kolestasis, dan infeksi virus hepatitis B atau hepatitis C. MiRNA memiliki keterlibatan pada pasien sirosis hepatis melalui perannya pada sel stelata hepatik atau hepatic stellate cells (HSC), di mana miRNA dipercaya sebagai kunci utama dalam pemeliharaan sifat fenotip quiescent dari HSC. Peran miRNA dalam proses patogenesis fibrosis hati dan sebagai biomarker masih banyak diteliti hingga saat ini.
Kata kunci: Biomarker, fibrosis hati, HSC, microRNA, myofibroblast
PENDAHULUAN
Fibrosis hati merupakan konsekuensi umum dari kerusakan hati kronis yang disebabkan antara lain oleh alcoholic steatohepatitis (ASH), nonalcoholic fatty liver disease (NAFLD), kolestasis, dan infeksi virus hepatitis B atau hepatitis C. Fibrosis ditandai dengan adanya timbunan yang berlebihan dari protein fibrilar extracellular matrix (ECM), seperti kolagen I dan III di celah Disse.[1]
MicroRNA (miRNA atau miR) merupakan kelompok RNA endogen noncoding yang terdiri dari sekitar 22 nukleotida. MiRNA berperan penting sebagai regulator ekspresi gen pada messenger RNA (mRNA) target, melalui degradasi atau menekan translasi mRNA target. MiRNA terlibat dalam berbagai proses seluler, yaitu perkembangan, proliferasi, diferensiasi sel, apoptosis, dan respons terhadap stres. Gangguan pada miRNA baik berupa mutasi, delesi, peningkatan, atau penurunan ekspresi dapat mengakibatkan berbagai penyakit, antara lain kanker, penyakit jantung, hati, kulit, autoimun, inflamasi, dan gangguan saraf.[2]
Meskipun saat ini sudah terdapat banyak data yang mendokumentasikan peran miRNA seluler pada fibrosis hati, namun belum ada konsensus mengenai fungsi regulasinya. Berbagai macam miRNA berperan pada proses profibrotik maupun antifibrotik. Secara umum, miRNA memodulasi banyak tahapan perkembangan fibrosis, seperti aktivasi sel stelata hepatik atau hepatic stellate cell (HSC), proliferasi, migrasi, dan apoptosis.[3]
DEFINISI
Fibrosis hati mengacu pada akumulasi jaringan parut yang keras dan berserat di hati. Pembentukan jaringan parut ini merupakan respons normal tubuh terhadap cedera, namun pada organ hati, adanya fibrosis sel hati menjadi hal yang merugikan. Ketika sel hepatosit mengalami cedera akibat infeksi virus, konsumsi alkohol, toksin, trauma, atau faktor lainnya, sistem kekebalan diaktifkan untuk memperbaiki kerusakan. Cedera atau nekrosis hepatosit merangsang sel-sel imun inflamasi untuk melepaskan sitokin, growth factor, dan senyawa lain.[4]
MicroRNA adalah noncoding single stranded RNA dengan panjang 18–25 nukleotida yang berfungsi sebagai molekul regulator dan terlibat dalam berbagai proses vital, antara lain proses diferensiasi, apoptosis, metabolisme, dan patogenesis dari berbagai macam penyakit pada manusia. MicroRNA telah terbukti memiliki peran yang signifikan pada penyakit hati.[5] MicroRNA pertama kali ditemukan pada nematoda Caenorhabditis elegans pada tahun 1993. Diketahui juga bahwa miRNA terdapat pada seluruh eukariota termasuk manusia. Sebagian besar miRNA pada mamalia berlokasi pada intron dan regio noncoding lainnya dari genom. Penamaan miRNA diikuti dengan serangkaian angka dan huruf berbeda yang menunjukkan identitas sekaligus urutan penemuannya. Sebagai contoh, miR-124 ditemukan lebih awal dari miR-456. MiRNA yang memiliki sekuens identik dengan beda panjang 1–2 nukleosida diidentifikasi dengan huruf kecil dibelakangnya, contohnya miR-124a dan miR-124b.[6]
BIOGENESIS miRNA
MicroRNA diproduksi melalui beberapa tahapan. Pertama, enzim RNA polymerase II ditranskripsi dari gennya dan kemudian akan menghasilkan prekursor 100 nukleotida berbentuk hairpin. Selanjutnya, 60–70 nukleotida dengan struktur yang lebih pendek yang disebut pre-miRNA, diproduksi di dalam nukleus oleh Drosha/RNAse III dengan bantuan DGCR8.[7]
Pada tahap selanjutnya, struktur tersebut akan masuk ke dalam sitoplasma dengan bantuan dari suatu protein membrane, yaitu exportin-5, untuk kemudian dikonversi menjadi miRNA dengan susunan 22–24 nukleotida oleh enzim Dicer/RNAse III. Kompleks lain yang disebut dengan RNA-induced silencing complex (RISC) akan membuat pre-miRNA untai ganda menjadi untai tunggal. Apabila untaian ini berikatan secara parsial pada 3’UTR, proses translasi mRNA menjadi protein akan dihambat, dan apabila untaian berikatan secara lengkap, fungsi mRNA akan dibatalkan sepenuhnya.[7]
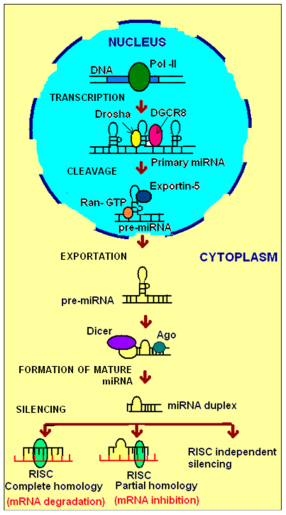
Gambar 1. Biogenesis miRNA.[8] (gambar diambil dari Sarkar N, Chakravarty R. 2015)
PATOGENESIS FIBROSIS HATI
Onset terjadinya fibrosis hati biasanya tidak diketahui dan terdeteksi. Morbiditas dan mortalitas akibat fibrosis hati terjadi setelah proses fibrosis berkembang menjadi sirosis dalam interval 15–20 tahun. Progresivitas tersebut dapat menjadi lebih cepat pada beberapa keadaan seperti hepatitis alkoholik akut berat, hepatitis subfulminan, dan kolestasis fibrosis.[9]
Pada organ hati yang normal, hepatic stellate cell (HSC) berada dalam kondisi tidak aktif (quiescent) dan nonproliferatif, dan bertugas menyimpan vitamin A dalam bentuk retinyl palmitate. Akan tetapi, ketika terjadi cedera hati akut ataupun kronis, HSC akan teraktivasi oleh transforming growth factor (TGF)-β dan bertransdiferensiasi menjadi sel myofibroblast yang ditandai dengan rendahnya jumlah vitamin A, tingginya ekskresi dari alpha smooth muscle actin (α-SMA) dan reseptor growth factor, serta peningkatan produksi kolagen. HSC yang teraktivasi juga akan mensekresikan sejumlah matrix metalloproteinases (MMPs) dan inhibitornya, yaitu tissue inhibitors of metalloproteinases (TIMPs).[9],[10]
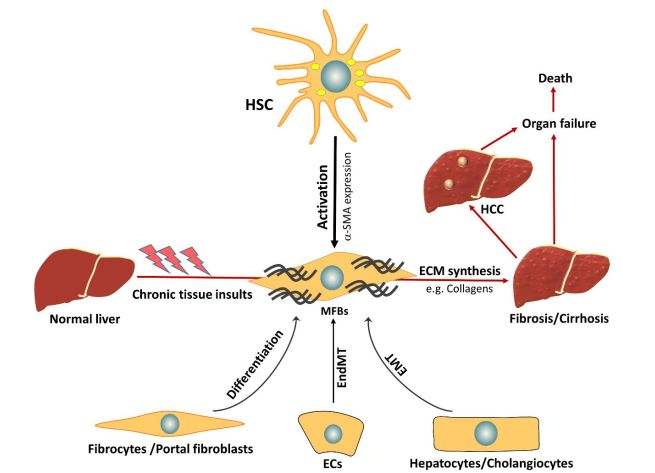
Gambar 2. HSC yang teraktivasi. (gambar diambil dari Dewidar B, et al. 2019)
Myofibroblast (MFB) adalah produsen utama kolagen, berbagai mediator fibrogenesis, komponen extracellular matrix (ECM), dan berperan dalam akumulasi mediator serta komponen pada jaringan luka di hati. MFB dapat berasal dari sumber yang berbeda, antara lain fibrosit derivat sumsum tulang, portal dan residen fibroblas, HSC yang teraktivasi dan berdiferensiasi, sel epitel hati (hepatosit dan kolangiosit) yang mengalami transisi epitelial-mesenkimal (EMT), sel endotel yang mengalami transisi endotelial-mesenkimal, sel otot polos vaskular, atau perisit.[1],[4],[11]
Berikut ini merupakan beberapa faktor yang memicu aktivasi HSC:[10]
1. Pola molekuler yang berkaitan dengan kerusakan, seperti protein yang berkaitan dengan kromatin, DNA dan RNA, dan reactive oxygen species (ROS) akibat kerusakan hepatosit.
2. Stimulus dari produksi parakrin, seperti ROS, sitokin platelet-derived growth factor (PDGF), TGF-β, sel Kupffer, kolangiosit, dan monosit kemotaktik protein-1 dari sel endotel sinusoid.
3. Molekul sinyal dari platelet dan sistem imun.
HSC yang teraktivasi akan mensekresikan peningkatan jumlah dari MMPs dan penghambatnya, serta TIMPs.
PERAN miRNA PADA FIBROSIS HATI
Berbagai penelitian mengungkapkan bahwa profil ekspresi miRNA menunjukkan ciri-ciri yang berhubungan dengan klasifikasi, diagnosis, dan perjalanan penyakit. Satu miRNA tunggal dapat meregulasi beberapa mRNA, sehingga kelainan pada satu miRNA dapat mengganggu ekspresi beberapa mRNA dan protein sekaligus. Sebagian besar miRNA bersifat spesifik pada suatu jaringan serta mengatur perkembangan lineage dan diferensiasi sel.[12]
Penelitian tentang keterlibatan miRNA pada pasien dengan sirosis hepatis menunjukkan adanya peran miRNA pada HSC. Penelitian oleh Coll (2015) berhasil mengidentifikasi miRNA yang memiliki peran kunci dalam mempertahankan fenotip quiescent dari HSC, yaitu miR-192. Terjadi down-regulasi miR-192 selama proses aktivasi quiescent HSC sehingga adanya over ekspresi miR-192 diduga memiliki peran penting dalam aktivasi HSC.[5]
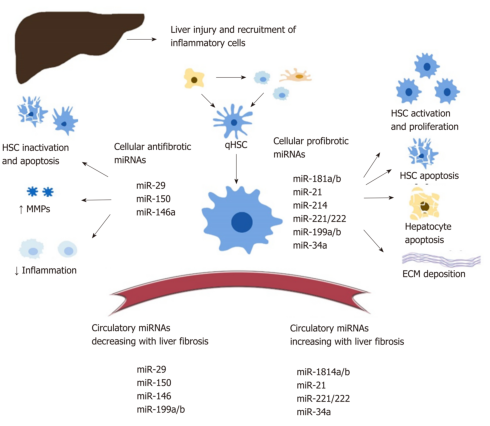
Gambar 3. Antifibrotik dan profibrotik miRNA pada proses fibrosis hati.3 (gambar diambil dari Iacob DG, et al. 2020)
Beberapa miRNA lain juga terlibat dalam aktivasi HSC, termasuk miR-199a, miR-21, miR-27, miR-125, miR-195, miR-221, dan miR-214 sebagai profibrotik miRNA. Sebaliknya, miR-29, miR-15b, miR-200, miR-133B, miR-122, dan miR-16 memiliki aktivitas antifibrotik.[10]
Penelitian lebih lanjut menunjukkan bahwa miR-30c dan miR-193 juga berperan pada regulasi TGF-β dalam mengontrol ekspresi gen ECM pada fibrosis yang diinduksi oleh CCl4. Ditemukan bahwa jumlah miR-30c dan miR-193 menurun selama proses fibrosis hepar. Oleh sebab itu, studi ini dengan jelas menyatakan bahwa miR-30c dan miR-193 memiliki peran dominan pada ekspresi gen yang berkaitan dengan ECM yang dimediasi oleh TGF-β, sehingga pada akhirnya akan mengaktivasi HSC dan mencetuskan fibrosis hati.[5]
Transforming growth factor beta (TGF-β) adalah sitokin profibrogenik yang dapat mengakibatkan fibrosis hati dengan cara menginduksi proliferasi HSC dan produksi ECM. Pada fibrosis hati hewan uji yang diinduksi oleh CCl4, miR-29 memediasi regulasi terjadinya fibrosis hati. MiR-29 dikatakan dapat meregulasi penurunan jumlah famili miR-29 yang bergantung pada TGF-β dan NF-κβ pada HSC, yang berakibat pada meningkatnya ekspresi gen yang berhubungan dengan ECM. Hasil temuan ini memiliki korelasi yang sesuai dengan studi klinis yang dilakukan pada pasien manusia dengan sirosis tahap lanjut yang menunjukkan adanya penurunan kadar serum miR-29a dibandingkan pada pasien dengan tahap awal fibrosis atau pada pasien sehat.[5]
PERAN miRNA SEBAGAI BIOMARKER
Pada tahun 2008, pertama kali terungkap bahwa miRNA dapat dideteksi dan diukur kadarnya dalam serum dan cairan tubuh lain sebagai cell-free miRNA. Adanya miRNA dalam serum menunjukkan miRNA resisten terhadap perombakan oleh RNAse. MiRNA juga stabil pada kondisi yang tidak menguntungkan, seperti suhu tinggi, pH rendah atau tinggi, dan kondisi lainnya. Hal ini diduga karena miRNA berada di dalam partikel (kompleks lipid atau lipoprotein) atau mikrovesikel (eksosom) yang melindungi terhadap degradasi oleh RNAse. Kemungkinan besar miRNA juga dapat ditemukan dalam cairan tubuh lain selain serum, karena mikrovesikel dan eksosom dapat dijumpai pada cairan tubuh lain.[12]
Peran miRNA sebagai biomarker yang potensial pada fibrosis hati masih dalam penelitian. Penelitian bioinformatika dan microarray mengungkapkan bahwa satu miRNA tunggal dapat berikatan dengan 200 gen sasaran yang berupa faktor transkripsi, reseptor, faktor yang disekresikan, maupun transporter.[12] Penggunaan biomarker miRNA sirkulasi pada praktik klinis masih memiliki kelemahan berupa rendahnya spesifisitas pada jaringan yang berbeda. Terkecuali miR-122 yang menyusun sekitar 70% dari semua miRNA yang terdapat pada hati, miRNA lainnya tidak spesifik berperan pada hati. Selain itu, signifikansi miRNA sirkulasi pada penyakit liver kronis juga dirumitkan dengan adanya perkembangan proses nekroinflamasi yang berjalan secara simultan serta adanya interaksi yang potensial antara sel host dan virus.[3]
Ekspresi individual miRNA pada serum dapat mencapai akurasi yang moderat untuk mendeteksi adanya fibrosis hati. Sebagai contoh adalah miR-29 yang dikenal sebagai miRNA antifibrotik. Berbagai penelitian menunjukkan angka miR-29 dibawah kurva adalah di antara 0,619 hingga 0,838. Penggunaan beberapa miRNA atau kombinasi noncoding RNA dengan marker laboratorium lainnya dapat meningkatkan akurasi diagnosis dan prognosis secara signifikan. Sebuah meta analisis oleh Gou dkk, yang mengidentifikasi 8 panel miRNA sirkulasi yang dapat digunakan sebagai marker diagnosis sirosis hati, menunjukkan area dibawah kurva 0,93 dengan confidence interval 95%: 0,91–0,95.[3]
MiRNA pada sirkulasi yang didapatkan melalui plasma atau serum memiliki korelasi dengan keberadaan dan progresivitas fibrosis hati dan nekroinflamasi, serta dapat digunakan sebagai prediksi survival pada pasien dengan sirosis atau hepatocellular carcinoma (HCC). Zhou dkk. dalam penelitiannya menjelaskan bahwa hasil pemeriksaan microarray untuk mengukur kadar miRNA dapat digunakan sebagai marker untuk penyakit hati. Temuannya pada 7 kelompok miRNA, antara lain adalah miR-122, miR-192, miR-92, miR-223, miR-26a, miR-27a, dan miR-801 menunjukkan bahwa terdapat perbedaan yang bermakna antara kelompok pasien HCC dengan pasien hepatitis B kronis, sirosis, dan subjek sehat.7 Penelitian oleh Hayes dkk. juga menunjukkan bahwa miR-122, miR-22, dan miR-99a dapat meningkat hingga 1,5 kali lipat pada pasien dengan infeksi Hepatitis B sehingga berpotensi digunakan sebagai biomarker spesifik pada penyakit hati.[8]
KESIMPULAN
miRNA telah diketahui sebagai regulator kunci ekspresi gen. Gangguan pada miRNA baik berupa mutasi, delesi, peningkatan atau penurunan ekspresi dapat mengakibatkan berbagai penyakit. Adanya pola disregulasi pada ekspresi miRNA dapat menimbulkan beberapa konsekuensi medis seperti berbagai macam penyakit fibrosis hati dan sirosis. Penelitian tentang miRNA semakin berkembang dan menjadikan miRNA sebagai salah satu biomarker yang bisa diharapkan pada pemeriksaan fibrosis hati. Namun demikian, sampai sejauh ini masih perlu observasi lanjut yang lebih mendalam karena miRNA memiliki jenis dan aktivitas sel yang spesifik dengan target ekspresi yang sangat luas.
DAFTAR PUSTAKA:
1. Dewidar B, Meyer C, Dooley S, Meindl-Beinker N. TGF-β in heparic stellate cell activation and liver fibrogenesis-updated 2019. Cells. 2019;8:1-35.doi:10.3390/cells8111419.
2. Juwita J. MicroRNA-21, microRNA-155 dan microRNA-10B: bagaimana perannya pada kanker payudara. Jurnal Kedokteran Syah Kuala. 2017;17(2):119-25.doi: https://doi.org/10.24815/jks.v17i2.8991.
3. Iacob DG, Rosca A, Ruta SM. Circulating microRNA as non-invasive biomarkers for hepatitis virus liver fibrosis. World Journal of Gastroenterology. 2020;26(11);1113-27.doi:10.3748/wjg.v26.i11.1113.
4. Fabregat I, Caballero-Diaz D. Transforming growth factor-β-Induced cell plasticity in liver fibrosis and hepatocarcinogenesis. Frontiers in Oncology. 2018;8:1-18.doi:10.3389/fonc.2018.00357.
5. Ezilaharsan D. Role of microRNA in hepatic fibrosis progression. Journal of Applied Pharmaceutical Science. 2018;8(5):174-8.doi:10.7324/JAPS.2018.8524.
6. Angelina A, Kodariah R. Molekul regulator gen “microRNA”: peranan pada karsinogenesis dan potensinya sebagai marker keganasan. Pratista Patologi. 2016;5(1):52-8.
7. Moosavy SH, Nezatizadeh A, Davoodian P, Eftekhar E, Zare S, Nazarnezhad MA. MicroRNA biomarkers profiling in diagnosis and therapuetic management of hepatitis B virus infection. Journal of Biochemistri Technology. 2018;2:117-27.
8. Sarkar N, Chakravarty. Hepatitis B virus infection, microRNA and liver disease. International Journal of Molecular Sciences.2015;16:17746-62.doi:10.3390/ijms160817746.
9. Safitri F. Mekanisme regenerasi hati secara endogen pada fibrosis hati. Majalah Kedokteran Universitas Muhammadiyah Malang. 2018;2(4):9-26
10. Murakami, Y, Kawada N. MicroRNA in hepatic pathophysiology. Hepatology Research. 2017;47:60-69.doi:10.1111/hepr.12730.
11. Pellicoro A, Ramachandran P, Iredale JP, Fallowfield JA. Liver fibrosis and repair: immune regulation of wound healing in a solid organ. Nature Reviews Immunology. 2014;14:181-94.doi:10.1038/nri3623.
12. Kresno, SB. MicroRNA dan implikasinya pada kanker. Indonesia Journal of Cancer. 2011;5(3):119-27.
13. Rodriguez DVS, Monteiro VVS, Navegantes-Lima KC, Oliviera ALB, Gaspar SLF, Quadros LBG, et al. MicroRNA in cell cycle progression and proliferation: molecular mechanism and pathways. Non-coding RNA Investigation. 2018;2(28):1-19.doi:10.21037/ncri.2018.04.06.